题目内容
【题目】以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。
Ⅰ、制取氯化锌主要工艺如下:
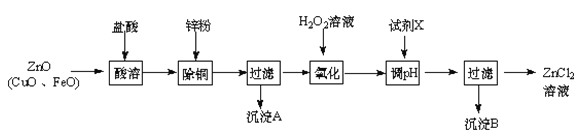
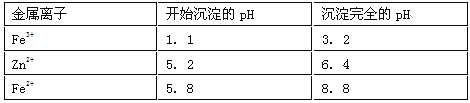
已知:Zn及化合物的性质与Al及化合物的性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
(1)加入H2O2溶液发生反应的离子方程式为 。
(2)流程图中,为了降低溶液的酸度,试剂X可以是 (选填序号:a.ZnO;b.Zn(OH)2 ;c.Zn2(OH)2CO3 ;d.ZnSO4);pH应调整到 。
(3)氯化锌能催化乳酸(![]() )生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ,聚乳酸的结构简式为 。
)生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ,聚乳酸的结构简式为 。
Ⅱ、制取金属锌采用碱溶解{ZnO(s)+2NaOH(aq)+H2O(l)=Na2[Zn(OH)4](aq)},然后电解浸取液。
(4)以石墨作电极电解时,阳极产生的气体为 ;阴极的电极反应为 。
(5)炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是 。
【答案】
(1)2Fe2+ +H2O2 +2H+ = 2Fe3++2H2O
(2)abc ;3.2 ≤ pH<5.2(或:约为4)
(3)![]() ;
;![]() (或:
(或:![]() )
)
(4)O2 (或氧气); [Zn(OH)4]2-+2e-=Zn+4OH-
(5)氧化铜、氧化亚铁不溶于碱溶液中
【解析】
试题分析:炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)加盐酸溶解,形成氯化锌、氯化铜、氯化亚铁的溶液,加锌粉置换出Cu,过滤,滤液中含有锌离子和亚铁离子,加过氧化氢氧化,把亚铁离子氧化为铁离子,加ZnO(或氢氧化锌等)调节PH,铁离子转化为氢氧化铁沉淀,过滤除去沉淀,得到氯化锌溶液。
(1)加过氧化氢将亚铁离子氧化为铁离子,反应的离子方程式为:2Fe2+ +H2O2 +2H+ = 2Fe3++2H2O;(2)调节pH时要消耗氢离子,但是不能引入杂质,ZnO、Zn(OH)2、Zn2(OH)2CO3均与氢离子反应生成锌离子,消耗氢离子的同时不引人杂质,ZnSO4不能与氢离子反应,所以不能调节pH,答案选abc;调节pH使铁离子转化为沉淀,而锌离子不沉淀,由表中数据可知pH≥3.2时,铁离子完全沉淀,而锌离子开始沉淀的pH为5.2,所以要调节pH为3.2≤pH<5.2;
(3)![]() 分子中含有-COOH和-OH,两分子的乳酸分子间发生酯化反应,反应产物为
分子中含有-COOH和-OH,两分子的乳酸分子间发生酯化反应,反应产物为![]() ;
;![]() 分子间发生缩聚反应生成聚乳酸和水,聚乳酸的结构简式为:
分子间发生缩聚反应生成聚乳酸和水,聚乳酸的结构简式为:![]() ;
;
(4)石墨作电极电解时,阳极氢氧根离子失电子,阳极反应为:4OH--4e-═2H2O+O2↑,所以阳极产生的气体是O2;阴极上[Zn(OH)4]2-得电子生成Zn,则阴极的电极方程式为:[Zn(OH)4]2-+2e-=Zn+4OH-。(5)ZnO能溶于强碱溶液,CuO和FeO不溶于碱溶液,酸溶液与ZnO、CuO、FeO均能反应,所以炼锌烟尘采用碱溶,而不采用酸溶后电解。

【题目】下表为元素周期表中的一部分。用化学式或元素符号回答下列问题:
IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)10种元素中,化学性质最不活泼的是__________(填元素名称)。
(2)三周期元素除⑩外原子半径最小的是______(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是__________(填化学式,下同),具有两性的是____________。
(3)在室温下有颜色的气体单质溶于水的离子方程式为_____ __;
(4)⑧与⑨分别与H2形成的氢化物的稳定性:__________,(用化学式表示)最高价氧化物对应的水溶液的酸性由强到弱的顺序:______ _________。(用化学式)
(5)①③⑤单质的活泼性顺序为_____>____>____(填元素符号),判断的实验依据是__(写出一种)