题目内容
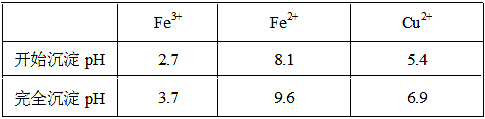
已知金属离子从开始形成氢氧化物沉淀到沉淀完全时溶液的pH。
(1)实验室配制FeCl2溶液时需加入少许盐酸和铁粉,若只加盐酸、不加铁粉,溶液中会发生什么变化,用离子方程式表示为: ;
(2)氯化铜晶体(CuCl2·2H2O)中含FeCl2杂质,为制得纯净氯化铜晶体,首先将其制成水溶液,然后按下面所示的操作步骤进行提纯。
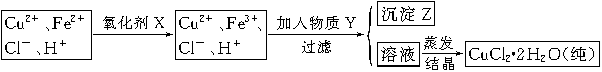
①加氧化剂X的目的是 ,下列氧化剂中最适合作氧化剂X的是 (填序号);
②物质Y的化学式是 ;加入物质Y的目的是调节溶液的pH至a,使Fe3+沉淀完全,则a的范围是 ;若25℃时,a=3的溶液中,c(Fe3+)= mol·L-1。(25℃时,Ksp[Fe(OH)3]=4.0×10-38)
(3)欲将CuCl2·2H2O加热制得无水CuCl2,将采用什么方法和措施?__________。

(1)实验室配制FeCl2溶液时需加入少许盐酸和铁粉,若只加盐酸、不加铁粉,溶液中会发生什么变化,用离子方程式表示为: ;
(2)氯化铜晶体(CuCl2·2H2O)中含FeCl2杂质,为制得纯净氯化铜晶体,首先将其制成水溶液,然后按下面所示的操作步骤进行提纯。

①加氧化剂X的目的是 ,下列氧化剂中最适合作氧化剂X的是 (填序号);
| A.NaClO | B.H2O2 | C.KMnO4 | D.HNO3 |
(3)欲将CuCl2·2H2O加热制得无水CuCl2,将采用什么方法和措施?__________。
(1)4Fe2++O2+4H+ 4Fe3++2H2O
4Fe3++2H2O
(2)①将Fe2+氧化为Fe3+ B ②CuO[或Cu(OH)2或CuCO3] 3.7≤a<5.4 4.0×10-5
(3)在HCl气氛下蒸发,以抑制CuCl2水解
 4Fe3++2H2O
4Fe3++2H2O(2)①将Fe2+氧化为Fe3+ B ②CuO[或Cu(OH)2或CuCO3] 3.7≤a<5.4 4.0×10-5
(3)在HCl气氛下蒸发,以抑制CuCl2水解
试题分析:(1)实验室配制FeCl2溶液时需加入少许盐酸和铁粉,目的是为了防止亚铁离子被氧化和析出沉淀,若只加盐酸、不加铁粉,溶液的亚铁离子被氧化为铁离子,其离子方程式为:4Fe2++O2+4H+
 4Fe3++2H2O;(2)氯化铜晶体(CuCl2·2H2O)中含FeCl2杂质,加氧化剂X的目的是将Fe2+氧化为Fe3+,最适合作氧化剂X的是H2O2,因为其氧化产物无污染,且容易除去;②物质Y是为了调节溶液的pH,并且不能引入新的杂质,或者是杂质很容易就除去了,故Y应该为CuO[或Cu(OH)2或CuCO3],右表可以看出,铁离子在pH为3.7时沉淀完全,而铜离子在5.4时才开始沉淀,故a的范围为3.7≤a<5.4;若25℃时,a=3的溶液中,则c (OH-)=10-11mol/L,c(Fe3+)=4.0×10-38/(10-11)3mol/L= 4.0×10-5 mol/L;(3)欲将CuCl2·2H2O加热制得无水CuCl2,因为其为强酸弱碱盐,所以必须在HCl气氛下蒸发,以抑制CuCl2水解。
4Fe3++2H2O;(2)氯化铜晶体(CuCl2·2H2O)中含FeCl2杂质,加氧化剂X的目的是将Fe2+氧化为Fe3+,最适合作氧化剂X的是H2O2,因为其氧化产物无污染,且容易除去;②物质Y是为了调节溶液的pH,并且不能引入新的杂质,或者是杂质很容易就除去了,故Y应该为CuO[或Cu(OH)2或CuCO3],右表可以看出,铁离子在pH为3.7时沉淀完全,而铜离子在5.4时才开始沉淀,故a的范围为3.7≤a<5.4;若25℃时,a=3的溶液中,则c (OH-)=10-11mol/L,c(Fe3+)=4.0×10-38/(10-11)3mol/L= 4.0×10-5 mol/L;(3)欲将CuCl2·2H2O加热制得无水CuCl2,因为其为强酸弱碱盐,所以必须在HCl气氛下蒸发,以抑制CuCl2水解。点评:本题考查了盐类水解,溶度积等知识点,这些考点都是高考考查的重点和难点,本题有一定的综合性,关键是要根据表中的数据进行解答,本题难度中等。

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
 CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。
 NH4++OH- ,当其他条件不变时,改变下列条件,平衡向左移动,且NH4+浓度增大的是( )
NH4++OH- ,当其他条件不变时,改变下列条件,平衡向左移动,且NH4+浓度增大的是( )