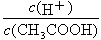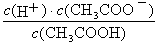题目内容
醋酸和盐酸是中学化学中常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。
(1)常温下,在 pH =5的稀醋酸溶液中,c(CH3COO-)=____________(列式,不必化简);下列方法中,可以使0.10 mol·L-1 CH3COOH的电离程度增大的是______?
a.加入少量0.10 mol·L-1的稀盐酸 b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量0.10 mol·L-1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V(盐酸)_________V(醋酸),反应的最初速率为:v(盐酸)_________v(醋酸)。(填写“>”、“<”或“=”)
(3)某同学用0.1000mol/LNaOH溶液分别滴定20.00mL 0.1000mol/LHCl和20.00mL0.1000mol/L CH3COOH,得到如图所示两条滴定曲线,请完成有关问题:

①NaOH溶液滴定CH3COOH溶液的曲线是 (填“图1”或“图2”);
②a= mL。
(4)常温下,将0.1 mol/L盐酸和0.1 mol/L醋酸钠溶液混合,所得溶液为中性,则混合溶液中各离子的浓度按由大到小排序为_______________________________。
(5)已知:90℃时,水的离子积常数为Kw = 3.80×10-13,在此温度下,将pH=3的盐酸和
pH = 11的氢氧化钠溶液等体积混合,则混合溶液中的c(H+)=____________(保留三位有效数字)mol/L。
 CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。(1)常温下,在 pH =5的稀醋酸溶液中,c(CH3COO-)=____________(列式,不必化简);下列方法中,可以使0.10 mol·L-1 CH3COOH的电离程度增大的是______?
a.加入少量0.10 mol·L-1的稀盐酸 b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量0.10 mol·L-1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V(盐酸)_________V(醋酸),反应的最初速率为:v(盐酸)_________v(醋酸)。(填写“>”、“<”或“=”)
(3)某同学用0.1000mol/LNaOH溶液分别滴定20.00mL 0.1000mol/LHCl和20.00mL0.1000mol/L CH3COOH,得到如图所示两条滴定曲线,请完成有关问题:

①NaOH溶液滴定CH3COOH溶液的曲线是 (填“图1”或“图2”);
②a= mL。
(4)常温下,将0.1 mol/L盐酸和0.1 mol/L醋酸钠溶液混合,所得溶液为中性,则混合溶液中各离子的浓度按由大到小排序为_______________________________。
(5)已知:90℃时,水的离子积常数为Kw = 3.80×10-13,在此温度下,将pH=3的盐酸和
pH = 11的氢氧化钠溶液等体积混合,则混合溶液中的c(H+)=____________(保留三位有效数字)mol/L。
(1)(10-5-10-9)mol/L(1分) bcf(1分)
(2)<(1分) =(1分)
(3)①图2 (1分) ②20.00(1分)
(4)c(Na+)>c(CH3COO-)>c(Cl-)>c(H+)= c(OH-)(1分)
(5)2.05×10-11(1分)
(2)<(1分) =(1分)
(3)①图2 (1分) ②20.00(1分)
(4)c(Na+)>c(CH3COO-)>c(Cl-)>c(H+)= c(OH-)(1分)
(5)2.05×10-11(1分)
试题分析:(1) pH =5的醋酸溶液中,氢离子的总的浓度为:10-5mol/L,但是由醋本身电离产生的氢离子浓度为总浓度与水所电离的氢离子浓度之差:(10-5-10-9)mol/L
(2) 等体积且pH均等于3的醋酸和盐酸溶液,醋酸所提供的氢离子的物质的量比盐酸的多。则生成氢气的体积:V(盐酸)<V(醋酸)。又因为二者的起始氢离子浓度,所以反应的最初速率为:v(盐酸=v(醋酸)。(3)浓度相等的盐酸和醋酸其PH值不等,可知NaOH溶液滴定CH3COOH溶液的曲线是图2。a点是刚好酸碱反应时的值,所以为20.00ml。(4)醋酸钠溶液显弱碱性,所以加入盐酸使其呈中性时的量就较小。因此有:
c(Na+)>c(CH3COO-)>c(Cl-)>c(H+)= c(OH-)
(5) 将pH=3的盐酸和pH = 11的氢氧化钠溶液等体积混合,溶液显碱性,所以应该先求此时溶液中的氢氧根离子的浓度,(假设二者各自的体积为V)
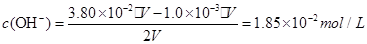
又因为在90℃时,水的离子积常数为Kw = 3.80×10-13,所以混合溶液中:


练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
 H++SO42-。
H++SO42-。 H++SO42-
H++SO42- H++SO42
H++SO42 HBr+OH-
HBr+OH-