题目内容
【题目】将W1g光亮的铜丝在空气中加热一段时间后,迅速伸入下列物质中,取出干燥,如此反复几次,最后取出铜丝用蒸馏水洗涤、干燥,称得其质量为W2g。实验时由于所伸入的物质不同,铜丝的前后质量变化可能不同,下列所插物质与铜丝的质量关系正确的是( )
A.NaOH溶液,W1=W2B.NaHSO4溶液,W1<W2
C.无水乙醇,W1=W2D.CO,W1>W2
【答案】C
【解析】
光亮的铜丝在空气中加热时,铜丝和氧气反应2Cu+O2![]() 2CuO生成黑色的氧化铜,所以加热后的铜丝质量会增加。
2CuO生成黑色的氧化铜,所以加热后的铜丝质量会增加。
A.NaOH溶液和CuO不反应,所以W2g为氧化铜的质量,W1g为铜丝的质量,所以W1<W2,故A错误;
B.2NaHSO4+CuO=CuSO4+Na2SO4+H2O,硫酸氢钠和氧化铜反应生成硫酸铜,所以有部分铜元素以离子方式进入溶液,W2g为未被氧化的铜质量,所以W1>W2,故B错误;
C.CH3CH2OH+CuO![]() CH3CHO+Cu+H2O,固体氧化铜又生成铜,所以W2g为铜的质量,W1g为铜的质量,所以W1=W2,故C正确;
CH3CHO+Cu+H2O,固体氧化铜又生成铜,所以W2g为铜的质量,W1g为铜的质量,所以W1=W2,故C正确;
D.氧化铜和CO反应生成固体铜,所以W2g为铜的质量,W1g为铜的质量,所以W1=W2,故D错误;
故答案为C。

 名校课堂系列答案
名校课堂系列答案【题目】类推思维是化学解题中常用的一种思维方法,下列有关反应方程式的类推正确的是
已知 | 类推 | |
A | 将Fe加入CuSO4溶液中Fe+Cu2+===Cu+Fe2+ | 将Na加入到CuSO4溶液中2Na+Cu2+===Cu+2Na+ |
B | 稀硫酸与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-===BaSO4↓+2H2O | NaHSO4溶液与Ba(OH)2溶液反应至中性2H++SO42-+Ba2++2OH-===BaSO4↓+2H2O |
C | 铁和氯气反应2Fe+3Cl2 | 铁和碘单质反应2Fe+3I2 |
D | 向Ca(ClO)2溶液中通入少量CO2:Ca2++2ClO-+CO2+H2O===CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClO |
A. A B. B C. C D. D
【题目】含锌废渣及粉尘是危险废物,碱浸电解法处理可得锌粉。但若其中存在氯,则锌质量就严重下降,对电极板也有严重腐蚀作用。工业上模拟碱浸电解法处理含锌质量分数为16%的废料(主要成分为ZnO、Zn(OH)2、ZnSO4及PbCO3、Fe2O3、Cu杂质)工艺如图:
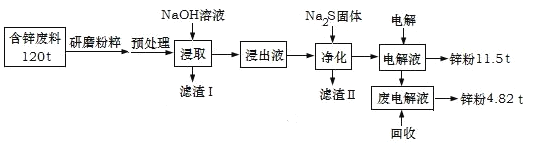
ⅰ.浸出液中含有[Zn(OH)4]2-和[Pb(OH)4]2-等离子
ⅱ.滤渣Ⅱ的主要成分为:Na2Pb(OH)xS![]()
(1)从物质分类的角度看,ZnO属于__,其与NaOH溶液发生反应的离子方程式为__。
(2)“滤渣Ⅰ”的主要成分为___。
(3)下表是“预处理”的2种除氯方案中粉尘氯的去除率和锌损失率分析表格可知,首选的“除氯剂”为___,原因是____。
除氯剂 | 碱(NaOH) | 碳酸钠 |
氯去除率/% | 78.75 | 83.69 |
锌损失率/% | 0.26 | 0.28 |
价格/t | 7200元 | 3600元 |
(4)“电解”过程中阴极的电极反应式为____。
(5)锌的总回收率为____。