题目内容
【题目】钠离子电池成本低、安全性好,有望在未来取代锂离子电池,某新型可充电钠离子电池放电的工作原理如图所示。下列分析错误的是( )
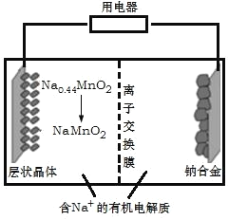
A. 出于环保考虑,应尽量避免使用重金属(如Pb)作为钠的合金化元素
B. 放电时,Na+由右室移向左室
C. 放电时,正极反应式为:Na0.44MnO2+0.56e-+0.56Na+=NaMnO2
D. 充电时,阴极质量变化4.6g时,外电路中通过0.1mole-
【答案】D
【解析】
A. Pb是重金属元素有毒,易造成环境污染,A正确;
B. 根据图示原电池放电时,左室Mn的化合价降低,得电子,发生还原反应,因此层状晶体做正极,钠合金做负极,Na+向正极移动,即Na+由右室移向左室,B正确;
C. 原电池放电时放电时,层状晶体做正极,根据图示,正极反应式为:Na0.44MnO2+0.56e-+0.56Na+=NaMnO2,C正确;
D. 充电时,阴极质量变化4.6g时,即有4.6g的钠元素质量发生变化,为0.2mol的钠离子变成钠单质,外电路中通过0.2mole-,D错误。
答案选D。

练习册系列答案
相关题目