题目内容
【题目】在一块表面无锈的铁片上滴食盐水,放置一段时间后看到铁片上有铁锈出现。铁片腐蚀过程中发生反应的总化学方程式:2Fe+2H2O+O2=2Fe(OH)2,Fe(OH)2进一步被氧气氧化为Fe(OH)3,再在一定条件下脱水生成铁锈,其原理如图所示。下列说法正确的是
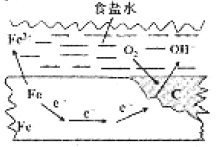
A. 铁片发生还原反应而被腐蚀
B. 铁片腐蚀生成的铁锈可以保护内层的铁不被腐蚀
C. 铁片腐蚀过程中负极发生的电极反应:2H2O+O2+4e-=4OH-
D. 铁片里的铁和碳与食盐水形成了无数微小原电池,发生了电化学腐蚀
【答案】D
【解析】
A.根据总反应方程式来看,铁失电子,所以铁发生氧化反应,A项错误;
B.铁片生成的铁锈是疏松多孔的,不能保护内层的铁,B项错误;
C.氧气得电子发生还原反应,所以氧气应是在正极反应,而不是负极,C项错误;
D.铁和碳分布不均匀,所以各个部分都可以与食盐水形成无数微小原电池,D项正确;
答案选D。

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目