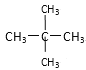
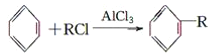题目内容
【题目】含锌废渣及粉尘是危险废物,碱浸电解法处理可得锌粉。但若其中存在氯,则锌质量就严重下降,对电极板也有严重腐蚀作用。工业上模拟碱浸电解法处理含锌质量分数为16%的废料(主要成分为ZnO、Zn(OH)2、ZnSO4及PbCO3、Fe2O3、Cu杂质)工艺如图:
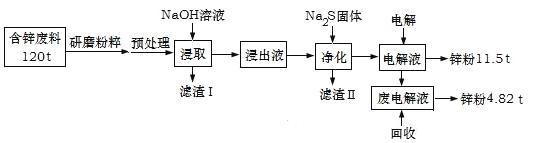
ⅰ.浸出液中含有[Zn(OH)4]2-和[Pb(OH)4]2-等离子
ⅱ.滤渣Ⅱ的主要成分为:Na2Pb(OH)xS![]()
(1)从物质分类的角度看,ZnO属于__,其与NaOH溶液发生反应的离子方程式为__。
(2)“滤渣Ⅰ”的主要成分为___。
(3)下表是“预处理”的2种除氯方案中粉尘氯的去除率和锌损失率分析表格可知,首选的“除氯剂”为___,原因是____。
除氯剂 | 碱(NaOH) | 碳酸钠 |
氯去除率/% | 78.75 | 83.69 |
锌损失率/% | 0.26 | 0.28 |
价格/t | 7200元 | 3600元 |
(4)“电解”过程中阴极的电极反应式为____。
(5)锌的总回收率为____。
【答案】两性氧化物 ![]() Fe2O3、Cu 碳酸钠 碳酸钠既能达到很好除氯效果又不会引起较大的锌损失,且比NaOH价格便宜
Fe2O3、Cu 碳酸钠 碳酸钠既能达到很好除氯效果又不会引起较大的锌损失,且比NaOH价格便宜 ![]() 85%
85%
【解析】
(1)ZnO既可以和酸反应,又可以和碱反应从物质分类的角度看,属于两性氧化物,其与NaOH溶液发生反应的离子方程式为![]() 。
。
(2)由于浸出液中含有[Zn(OH)4]2-和[Pb(OH)4]2-等离子,所以“滤渣Ⅰ”的主要成分为Fe2O3、Cu。
(3)分析表格可知,首选的“除氯剂”为碳酸钠,原因是碳酸钠既能达到很好除氯效果又不会引起较大的锌损失,且比NaOH价格便宜。
(4)“电解”过程产物为锌粉,[Zn(OH)4]2-在阴极得电子产生锌单质,电极反应式为![]() 。
。
(5)废料中含锌的总质量=120t![]() 16%=19.2 t,通过流程共回收锌的质量=11.5 t+4.82 t=16.32 t,锌的总回收率=
16%=19.2 t,通过流程共回收锌的质量=11.5 t+4.82 t=16.32 t,锌的总回收率=![]() =85%
=85%