题目内容
11.下列对强、弱电解质的描述,不正确的是( )| A. | 强电解质是指在水溶液中能完全电离的电解质 | |
| B. | 在水溶液中离子浓度小的电解质为弱电解质 | |
| C. | 在水溶液中只能部分电离的电解质为弱电解质 | |
| D. | 强酸、强碱和绝大部分盐类为强电解质 |
分析 电解质依据在水溶液中电离程度分为强电解质,弱电解质,在水溶液能够完全电离的属于强电解质,强电解质包括:强酸、强碱和绝大部分盐类、活泼金属氧化物;只能部分电离是属于弱电解质,弱电解质包括:弱酸、弱碱和水;电解质的强弱与溶解性、导电能力大小无关,据此解答.
解答 解:A.依据强电解质概念可知:强电解质是指在水溶液中能完全电离的电解质,故A正确;
B.电解质的强弱取决于电解质在水中电离程度,与离子浓度大小无关,故B错误;
C.依据弱电解质概念可知:在水溶液中只能部分电离的电解质为弱电解质,故C正确;
D.强酸、强碱和绝大部分盐类为强电解质,故D正确;
故选B
点评 本题考查了电解质强弱的理解,明确电解质强弱判断依据是解题关键,注意电解质强弱与电离程度有关与离子浓度、溶解性、导电性强弱无关,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列各种粒子,在氧化还原反应中通常只可作为氧化剂使用的是( )
| A. | SO32- | B. | MnO4- | C. | Cl- | D. | Fe |
2.已知:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98kJ/mol.某温度下,向一体积为2L的密闭容器中充入0.2mol SO2和0.1mol O2,5min达到平衡,放出热量11.76kJ,下列说法正确的是( )
| A. | 5 min内用O2表示的反应速率为0.12 mol/(L•min) | |
| B. | 该反应的平衡常数数值为7.5 | |
| C. | SO2的平衡转化率为60% | |
| D. | 加入催化剂,可使△H变小 |
19.氯气是一种重要的化工原料,除了用于制备盐酸和漂白剂外,还用于制备有机溶剂和杀菌消毒剂等.下列有关氯气的叙述中,正确的是( )
| A. | 氯气、氯水、液氯是同一种物质,只是状态不同 | |
| B. | 氯气不能溶于水,所以可以用排水法收集 | |
| C. | 氯气是一种黄绿色、有刺激性气味的气体 | |
| D. | 用自来水配制AgNO3溶液时,药品不会变质 |
6.化学反应有自身规律,下列有关化学分应的叙述正确的是( )
| A. | 将二氧化碳通入次氯酸钙溶液可生成次氯酸 | |
| B. | 锂在氧气中燃烧主要生成Li2O2 | |
| C. | 二氧化硫通入氯化钙溶液可生成CaSO2沉淀 | |
| D. | 氯气通入硫酸铜溶液中能使Cu2+还原成Cu |
16.下列有关化学用语中最能体现氮原子核外电子运动状态的是( )
| A. | 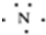 | B. |  | ||
| C. | 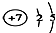 | D. | 1s22s22p3 |
1.将金属钠分别投入下列物质的稀水溶液中:①HCl ②K2SO4③MgCl2④CuCl2,能生成沉淀的是( )
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
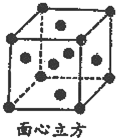 金属及其化合物在科学研究和工业生产中具有许多用途.回答下列问题:
金属及其化合物在科学研究和工业生产中具有许多用途.回答下列问题: