题目内容
实验室用足量镁粉与一定量的某浓度的盐酸反应来制得氢气。由于反应速率太快,不易操作。为减慢反应速率,同时又不影晌生成H2的总置,可向盐酸中加入的物质是
| A.CH3COONa固体 | B.NaOH溶液 | C.(NH4)2SO4粉末 | D.K2SO4固体 |
A
为减慢反应速率,同时又不影晌生成H2的总置,可向盐酸中加入CH3COONa固体,强酸变成弱酸,速率减慢。NaOH溶液、(NH4)2SO4粉末消耗氢离子影响氢气的质量;K2SO4固体加入不改变速率。

练习册系列答案
相关题目
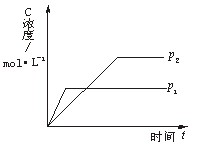
 nC(g) (正反应放热)生成物C的浓度随压强变化并建立平衡的关系图,则n值与压强P1、P2的关系正确的是
nC(g) (正反应放热)生成物C的浓度随压强变化并建立平衡的关系图,则n值与压强P1、P2的关系正确的是