题目内容
9.乙二酸俗称草酸,为二元酸(结构简式为HOOC-COOH,可简写为H2C2O4).25℃时,草酸的电离平衡常数K1=5.0×10-2,K2=5.4×10-5;碳酸的电离平衡常数K1=4.5×10-7,K2=4.7×10-11.草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9.回答下列问题:(1)写出水溶液中草酸的电离方程式:H2C2O4?HC2O4-+H+、HC2O4-?C2O42-+H+.
(2)25℃,物质的量浓度都为0.1mol/L的Na2C2O4溶液的pH比Na2CO3溶液pH小(填“大”“小”或“相等”).
(3)常温下将0.2mol/L的KOH溶液10mL与0.2mol/L的草酸溶液10mL混合,若混合溶液显酸性,则该溶液中所有离子浓度由大到小的顺序:c(K+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-).
(4)25℃时向20mL碳酸钙的饱和溶液中逐滴加入1.0×10-3 mol/L的草酸钾溶液20mL,能否产生沉淀?否(填“能”或“否”).
(5)除去锅炉水垢中的CaSO4可先用碳酸钠溶液处理,而后用盐酸溶解,其反应的离子方程式:CaSO4+CO32-=CaCO3+SO42-;CaCO3+2H+=Ca2++H2O+CO2↑.
分析 (1)草酸是二元弱酸,分步电离;
(2)相同条件下,酸的电离平衡常数越大,其电离程度越大,则酸根离子的水解程度越大,溶液的碱性越强;
(3)将0.2mol/L的KOH容液10mL与0.2mol/L的草酸溶液10mL混合,恰好完全反应生成KHC2O4,结合溶液的酸碱性比较离子浓度大小;
(4)根据c(Ca2+)•c (C2O42-)和Ksp(4.0×10-8)相对大小判断,如果c(Ca2+)•c (C2O42-)=<Ksp(4.0×10-8),则无沉淀生成;
(5)水垢中含有的CaSO4,先用碳酸钠溶液处理,转化为 CaCO3,再和盐酸反应得到氯化钙、水以及二氧化碳.
解答 解:(1)草酸是二元弱酸,在水溶液里存在两步电离,第一步电离程度大于第二步,其电离方程式分别为:H2C2O4?HC2O4-+H+、HC2O4-?C2O42-+H+,
故答案为:H2C2O4?HC2O4-+H+、HC2O4-?C2O42-+H+;
(2)草酸的第二步电离平衡常数大于碳酸的第二步电离平衡常数,电离平衡常数越小,其酸根离子的水解程度越大,所以碳酸根离子的水解程度大于草酸根离子,导致草酸钠的pH小于碳酸钠,
故答案为:小;
(3)将0.2mol/L的KOH容液10mL与0.2mol/L的草酸溶液10mL混合,恰好完全反应生成KHC2O4,存在的离子是H+、HC2O4-、C2O42-、H2C2O4、OH-,若混合溶液显酸性,说明HC2O4-电离程度大于水解程度,则C2O42->H2C2O4溶液还存在水的电离,则H+>C2O42-,离子浓度的顺序为:c(K+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-),
故答案为:c(K+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-);
(4)碳酸钙溶液中钙离子浓度=$\sqrt{2.5×1{0}^{-9}}$mol/L=5×10-5mol/L,二者混合后,钙离子浓度=2.5×10-5mol/L,草酸钾的浓度为5.0×10-4 mol/L,混合后c(Ca2+)•c (C2O42-)=2.5×10-5 ×5.0×10-4=1.25×10-8<Ksp(4.0×10-8),故无沉淀,
故答案为:否;
(5)水垢中含有的CaSO4,先用碳酸钠溶液处理,转化为 CaCO3,转化的离子方程式是CaSO4(s)+CO32- (aq)?CaCO3(s )+SO42- (aq),CaCO3+2H+=Ca2++H2O+CO2↑,
故答案为:CaSO4+CO32-=CaCO3+SO42-;CaCO3+2H+=Ca2++H2O+CO2↑.
点评 本题考查了弱电解质的电离、难溶物的溶解平衡,为高频考点,侧重于学生的分析能力和计算能力的考查,明确弱电解质电离特点及溶度积常数的运用是解本题关键,难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案①CH2=CHCOOH
②CH2=CHOOCH3
③CH2=CHCH2OH
④CH3CH2CH2OH
⑤
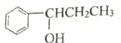
| A. | ①③④ | B. | ②④⑤ | C. | ①③⑤ | D. | ①②⑤ |
(1)按物质的分类方法填写表格的空白处(填写序号):1⑦⑧⑨;2③④;3③⑤⑥⑩;
| 分类标准 | 混合物 | 氧化物 | 电解质 |
| 属于该类的物质 | 1 | 2 | 3 |
(3)写出下列物质之间反应的离子方程式:少量的④通入⑥的水溶液CO2+Ba2++2OH-═BaSO4↓+H2O;⑤的水溶液与⑥的水溶液混合2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O;
(4)质量都是10g的HCl、NH3、CO2、H2四种气体在标准状况下,体积最小的是CO2,密度最小的是H2;(填分子式)
(5)②与⑨发生反应的化学方程式为:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,HNO3是氧化剂,Cu元素被氧化,参加反应的HNO3中,n(HNO3)被还原:n(HNO3)未被还原=1:3,当有6.4gCu发生反应时,转移电子的物质的量为0.2mol.
| A. | 22.4L氯气中所含分子数为NA | |
| B. | 标准状况下2.24LH2O所含原子数为0.3NA | |
| C. | 1L1mol/LFeCl3溶液所含Cl-数目为NA | |
| D. | 一定条件下1molH2和1molCl2充分反应后生成HCl分子数为2NA |
| A. | ①和② | B. | ①和③ | C. | ②和③ | D. | ②和④ |
 图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答:
图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答: