题目内容
17.向沸水中滴加FeCl3溶液并继续煮沸至液体呈透明的红褐色即可制得Fe(OH)3胶体,反应方程式为:FeCl3+3H2O═Fe(OH)3(胶体)+3HCl,制得的胶体常混有FeCl3和HCl,试回答:(1)鉴别是否得到胶体的方法是:用一束光照射,观察是否有光亮的通路;
(2)除去混在胶体中FeCl3和HCl的方法是:渗析.
分析 (1)丁达尔现象为胶体特有的性质,以此检验;
(2)胶粒不能透过半透膜.
解答 解:(1)用一束光照射,观察是否有光亮的通路,可检验是否为胶体,故答案为:用一束光照射,观察是否有光亮的通路;
(2)除去胶体中的电解质可利用构成它们粒子的大小不同,通过渗析来分离,故答案为:渗析.
点评 本题考查物质的鉴别和分离提纯,侧重胶体性质的考查,注意丁达尔现象(效应)是鉴别溶液和胶体的最简单的方法,题目较简单.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案
相关题目
7.物质的量浓度相同的三种正盐NaX、NaY、NaZ的水溶液,其pH分别为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是( )
| A. | HX,HZ,HY | B. | HX,HY,HZ | C. | HZ,HY,HX | D. | HY,HZ,HX |
8.下列反应类型中属于化学平衡主要研究对象的是( )
| A. | 化合反应 | B. | 离子反应 | C. | 可逆反应 | D. | 气体反应 |
2.下列实验操作中有错误的是( )
| A. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时,温度计水银球应浸没在液体中 | |
| C. | 蒸馏中,冷却水应从冷凝管的下口通入,上口流出 | |
| D. | 把几滴FeCl3饱和溶液滴入250mL沸水中继续煮沸至红褐色制取Fe(OH)3胶体 |
6.下列物质组合中,既能和强酸反应又能和强碱反应的物质是( )
①Al ②Al2O3 ③Al(OH)3 ④AlCl3⑤NaHCO3.
①Al ②Al2O3 ③Al(OH)3 ④AlCl3⑤NaHCO3.
| A. | ①②③⑤ | B. | ②③④ | C. | ①②④ | D. | ①② |
7.下列叙述正确的是( )
| A. | 1molH2O的质量为18g•mol-1 | |
| B. | CH4的摩尔质量为16g | |
| C. | 3.01×1023个SO2分子的质量为32 g | |
| D. | 1mol任何物质均含有6.02×1023个分子 |
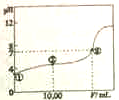 常温下,将0.1000mol.L-1NaOH溶液滴入20.00mL0.1000mol.L-1的一元酸HA溶液中,测得混合溶液的pH变化曲线如下图所示.
常温下,将0.1000mol.L-1NaOH溶液滴入20.00mL0.1000mol.L-1的一元酸HA溶液中,测得混合溶液的pH变化曲线如下图所示.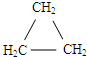 d.CH2=CHCH3.
d.CH2=CHCH3.