题目内容
5.下列装置能达到相应实验目的是( )
| A. | 甲用于浓盐酸和漂粉精制取并收集干燥的Cl2 | |
| B. | 乙用于测定盐酸的浓度 | |
| C. | 丙用于证明浓硫酸具有脱水性和强氧化性 | |
| D. | 丁用于制取金属镁 |
分析 A.氯气密度比空气大,应用向上排空法收集;
B.氢氧化钠应放在碱式滴定管中;
C.浓硫酸具有脱水性,可使蔗糖碳化而变黑,生成二氧化硫,可使高锰酸钾褪色;
D.镁比铝活泼,铝不能置换出镁.
解答 解:A.氯气微溶于水,应用饱和食盐水除去氯化氢,且氯气密度比空气大,应用向上排空法收集,故A错误;
B.氢氧化钠可腐蚀玻璃塞,应放在碱式滴定管中,故B错误;
C.浓硫酸具有脱水性,可使蔗糖碳化而变黑,与碳发生氧化还原反应生成二氧化硫,可使高锰酸钾褪色,故C正确;
D.镁比铝活泼,铝不能置换出镁,故D错误.
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及气体的制取、中和滴定、性质检验以及金属冶炼等,把握实验原理及实验装置图的作用为解答的关键,注意方案的合理性、操作性分析,题目难度不大.

练习册系列答案
相关题目
16.X、Y、Z是三种主族元素,如果Xn+阳离子与Yn-阴离子具有相同的电子层结构,Zn-阴离子半径大于Yn-阴离子半径,则三种元素的原子序数由大到小的顺序是( )
| A. | Z>X>Y | B. | X>Y>Z | C. | Z>Y>X | D. | X>Z>Y |
13.下列说法正确的是( )
| A. | 容量瓶、分液漏斗、滴定管在使用前都需要检查是否漏水,可以用相同的实验方法检查是否漏水 | |
| B. | 溶液蒸发操作时蒸发皿中液体的量不能超过容积的$\frac{1}{2}$ | |
| C. | 强酸滴定强碱时,用酚酞指示剂比用甲基橙更易判断滴定终点 | |
| D. | 将灼烧后的海带灰加水煮沸2-3分钟的目的是加快碘化物在水中的溶解,使灰烬中的碘离子尽可能多的进入溶液 |
10.下列关于有机物同分异构体的说法正确的是( )
| A. | C4H10的二氯取代物有4种 | |
| B. | 最简式为C2H5的烃结构简式有5种 | |
| C. | 乙苯的一氯取代物只有3种 | |
| D. | 分子式为C4H10O且与钠反应的有机物有4种 |
14.欲将AlCl3溶液中的铝离子沉淀完全,最合适的试剂是( )
| A. | NaOH溶液 | B. | 氨水 | C. | AgNO3溶液 | D. | NaCl溶液 |
15.在常温条件下,下列对醋酸的叙述中,不正确的是( )
| A. | pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-) | |
| B. | 将pH=a的醋酸稀释为pH=a+1的过程中,$\frac{{cCH}_{3}COOH}{{cH}^{+}}$变小 | |
| C. | 浓度均为0.1 mol•L-1的CH3COOH和CH3COONa溶液等体积混合后:c(CH3COO-)-c(CH3COOH)=2c(H+)-c(OH-) | |
| D. |  向10.00 mL 0.1 mol•L-1HCOOH溶液中逐滴加入0.1 mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化),则c点NaOH溶液的体积小于10 mL 向10.00 mL 0.1 mol•L-1HCOOH溶液中逐滴加入0.1 mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化),则c点NaOH溶液的体积小于10 mL |
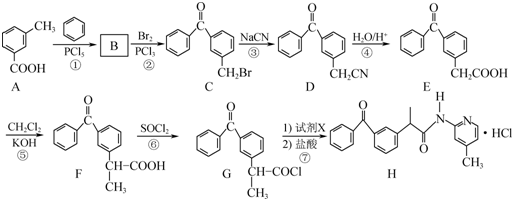
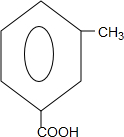 +
+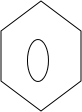 $\stackrel{PCl_{3}}{→}$
$\stackrel{PCl_{3}}{→}$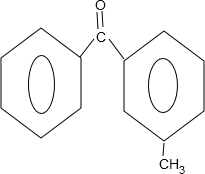 +H2O.
+H2O.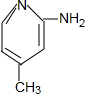 .
.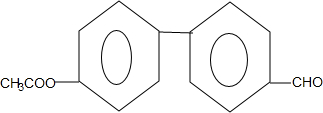 (只写一种).
(只写一种).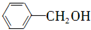 和
和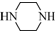 为原料制备
为原料制备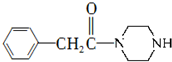 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).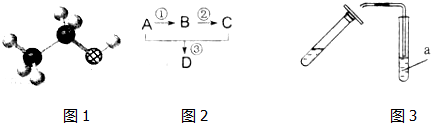

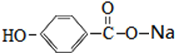 的化学试剂是NaHCO3(写化学式).
的化学试剂是NaHCO3(写化学式). ,E转化为F的化学反应类型是酯化反应或取代反应.
,E转化为F的化学反应类型是酯化反应或取代反应. +3NaOH$\stackrel{△}{→}$HOCH2CH2OH+NaCl+
+3NaOH$\stackrel{△}{→}$HOCH2CH2OH+NaCl+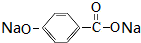 +H2O.
+H2O. .
.