题目内容
15.在常温条件下,下列对醋酸的叙述中,不正确的是( )| A. | pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-) | |
| B. | 将pH=a的醋酸稀释为pH=a+1的过程中,$\frac{{cCH}_{3}COOH}{{cH}^{+}}$变小 | |
| C. | 浓度均为0.1 mol•L-1的CH3COOH和CH3COONa溶液等体积混合后:c(CH3COO-)-c(CH3COOH)=2c(H+)-c(OH-) | |
| D. | 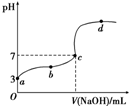 向10.00 mL 0.1 mol•L-1HCOOH溶液中逐滴加入0.1 mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化),则c点NaOH溶液的体积小于10 mL 向10.00 mL 0.1 mol•L-1HCOOH溶液中逐滴加入0.1 mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化),则c点NaOH溶液的体积小于10 mL |
分析 A.根据电荷守恒分析;
B.加水稀释促进电离;
C.物质的量浓度均为0.1mol/L的CH3COONa和CH3COOH溶液等体积混合,溶液显酸性,电荷守恒为c(Na+)+c(H+)=c(CH3COO-)+c(OH-),物料守恒为c(CH3COO-)+c(CH3COOH)=0.1mol/L=2c(Na+);
D.假设c点NaOH溶液的体积为10 mL,则甲酸和NaOH恰好完全反应,所得HCOONa溶液显碱性,而图中c点显中性,据此分析.
解答 解:A.pH=5.6的CH3COOH与CH3COONa混合溶液中,电荷守恒为c(Na+)+c(H+)=c(OH-)+c(CH3COO-),pH=5.6,则c(H+>(OH-),所以c(Na+)<c(CH3COO-),故A正确;
B.加水稀释促进电离,则氢离子的物质的量增大,醋酸的物质的量减小,$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$=$\frac{n(C{H}_{3}COOH)}{n({H}^{+})}$变小,故B正确;
C.物质的量浓度均为0.1mol/L的CH3COONa和CH3COOH溶液等体积混合,溶液显酸性,电荷守恒为c(Na+)+c(H+)=c(CH3COO-)+c(OH-),物料守恒为c(CH3COO-)+c(CH3COOH)=0.1mol/L=2c(Na+),由上述两个式子可得c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)],故C错误;
D假设c点NaOH溶液的体积为10 mL,则甲酸和NaOH恰好完全反应,所得HCOONa溶液显碱性,而图中c点显中性,则NaOH溶液的体积小于10 mL,故D正确;
故选C.
点评 本题考查弱电解质的电离,侧重于学生的分析能力的考查,注意把握弱电解质的电离特点以及影响因素,题目难度中等.

 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案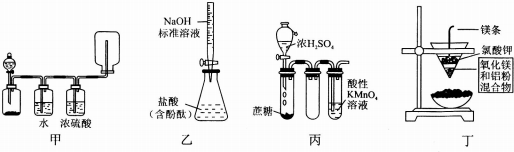
| A. | 甲用于浓盐酸和漂粉精制取并收集干燥的Cl2 | |
| B. | 乙用于测定盐酸的浓度 | |
| C. | 丙用于证明浓硫酸具有脱水性和强氧化性 | |
| D. | 丁用于制取金属镁 |
| A. | 将CO2通过Na2O2使其增重a g时,反应中转移电子数为$\frac{a{N}_{A}}{14}$ | |
| B. | 将1mol Cl2通入到水中,则N(HClO)+N(Cl-)+N(ClO-)=2NA | |
| C. | 常温常压下,3.0 g 含甲醛(HCHO)的冰醋酸中含有的原子总数为0.4NA | |
| D. | 2.24L的CH4中含有的C-H键数为0.4NA |
| A. | 常温常压下,1mol氦气含有的核外电子数为4NA | |
| B. | 常温常压下,17g甲基(-14CH3)所含的中子数为8NA | |
| C. | 0.44g C3H8中含有的共用电子对总数目为0.08NA | |
| D. | 常温常压下,100 mL 0.5 mol/L 的乙酸溶液中,乙酸的分子数目为0.05NA |
| A. | 镁铝合金既可完全溶于过量盐酸又可完全溶于过量NaOH溶液 | |
| B. | 在加入铝粉能放出氢气的溶液中,K+、NH4+、CO32-、Cl-一定能够大量共存 | |
| C. | 氯化铝溶液中加入过量氨水反应的实质:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 依据铝热反应原理,能发生反应2Al+3MgO$\frac{\underline{\;高温\;}}{\;}$3Mg+A12O3 |
| A. | 常温常压下,8g CH4含有4NA个氢原子 | |
| B. | 1mol Cu与足量FeCl3溶液反应,转移2NA个电子 | |
| C. | 1L0.1 mol•L-1(NH4)2SO4溶液中含有0.2NA个NH4+ | |
| D. | 10 L pH=l的硫酸溶液中含有的H+离子数为2NA |
| A. | 酸性氧化物的性质 | B. | 漂白性 | ||
| C. | 氧化性 | D. | 还原性 |
 .
.