��Ŀ����
����Ŀ��CO��NO��������β���е��к����ʣ�����֮���ܻ����ط������·�Ӧ��2NO(g)��2CO(g) ![]() N2(g)��2CO2(g)����H<0�������ô˷�Ӧ�������һ�ֻ���װ�ã�������������β���Դ�������Ⱦ��������Ʒ�����������Ч�����β������Ч������ (����)
N2(g)��2CO2(g)����H<0�������ô˷�Ӧ�������һ�ֻ���װ�ã�������������β���Դ�������Ⱦ��������Ʒ�����������Ч�����β������Ч������ (����)
��ѡ���ʵ��Ĵ����� �����װ���¶ȡ� ������װ�õ�ѹǿ�� ��װ���з����ʯ��
A. �٢� B. �ڢ� C. �� D. �ڢ�
���𰸡�A
��������Ҫ���β������Ч��,��Ҫβ���ŷŵ�����֮ǰ�����ܵ�ת��Ϊ������,Ӧ�����ʼ�ƽ��ĽǶȷ���: �ٴ���,���Լӿ췴Ӧ����,����Ӱ��ת����������¶�,�ܼӿ췴Ӧ����,���ή��ת�������۽���ѹǿ,�ȼ�����Ӧ����,�ֽ���ת�������ܷ����ʯ��,�����������ɵĶ�����̼,ʹƽ�������ƶ���
��ѡ���ʵ��Ĵ���,���Լӿ췴Ӧ����,����Ӱ��ת����,ʹ�к��������ų�֮ǰ�����ܵ�ת��Ϊ������,�������β������Ч������ȷ�������װ���¶�,��Ȼ�ܼӿ췴Ӧ����,�÷�Ӧ������ƽ�����������ή��ת����,�������۽���װ�õ�ѹǿ,�ȼ�����Ӧ����,�ֽ���ת��������������װ���з����ʯ��,�����������ɵĶ�����̼,ʹƽ�������ƶ�,���ת��������ȷ����������Ϊ�٢ܣ���ȷѡ��A��

����Ŀ��Cl2��һ����Ҫ�Ĺ�ҵԭ�ϣ�Һ�ȴ��������е�˵�������£�
��װ | ��ƿ |
����Ҫ�� | Զ�������ĩ���������ࡢ�������ʣ�������������� |
й©���� | NaOH��NaHSO3��Һ���� |
���н�����ʵ�ķ���ʽ����ȷ����
A. ��ⱥ��ʳ��ˮ��ȡCl2��2Cl�� +2H2O![]() 2OH��+ H2��+Cl2��
2OH��+ H2��+Cl2��
B. ������������ˮ������Cl2 + H2O![]() 2H+ + Cl��+ ClO��
2H+ + Cl��+ ClO��
C. Ũ��ˮ����й¶���������������̣�8NH3 + 3Cl2 === 6 NH4Cl + N2
D. ������й©��������NaHSO3��Һ�����ã�HSO3��+ Cl2 + H2O === SO42��+ 3H+ + 2Cl��
����Ŀ��ijѧϰС��̽��������������Һ�ķ�Ӧ��ʵ��������£�
ʵ����� | ʵ����� | ʵ������ |
I | ��һ�������ྻ����˿���뵽0.1mol/L ��AgNO3��Һ�� | ��˿����������ɫ������������Һ��Ϊdz��ɫ |
II | ȡ����ʵ��I���ϲ���Һ������K3[Fe(CN) 6]��Һ | ����ɫ�������� |
��1����������ʵ������ͬѧ��Ϊ��Fe2+���ɣ�������������Һ�ķ�Ӧ�����ӷ���ʽ��____________________��
��2����ͬѧ��Ϊʵ���п�������Fe3+����Ʋ��������ʵ��
ʵ����� | ʵ����� | ʵ������ |
III | ȡ����ʵ��I���ϲ���Һ����������KSCN��Һ���� | ������ɫ��������Һ�ֲ���죬���ɫ��ʧ������������ |
�������ϣ�Ag+��SCN�����ɰ�ɫ����AgSCN
��ͬѧ�ж���Fe3+�������� ____________________��
��3����ͬѧ����̽����ɫ��ȥ��ԭ����Ʋ��������ʵ��
ʵ����� | ʵ����� | ʵ������ |
IV | ȡ����ʵ��I���ϲ���Һ���μӼ���ϡ���� | �а�ɫ�������� |
V | ȡ1mLFe(NO3)3��Һ���μ�2�ε�Ũ�ȵ�KSCN��Һ�����ٵμ�����AgNO3��Һ | ��Һ��죻����Һ��ɫ�ޱ仯���μ�AgNO3����Һ��ɫ��ȥ��������ɫ������ |
�� ʵ��IV��Ŀ����____________________��
�� ��ƽ���ƶ�ԭ�����ͣ�ʵ��V����Һ��ɫ��ȥ��ԭ��____________________��
��4������Ϊ��Һ��Fe3+��Fe2+��Ag+�������¡�����ͼ����װ�ò�����ʵ�飬һ��ʱ���ȡ������ձ���Һ����KSCN��Һ����Һ���
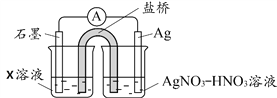
�� ����X��Һ��____________________��
�� ��ʵ��ó�Ag+��Fe2+��Ӧ�����ӷ���ʽ��____________________��
�� ��ͬѧ��ʵ����Ƽ������Ƿ��������˵������____________________��

