题目内容
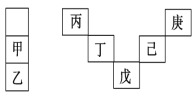
【题目】甲~庚等元素在周期表中的相对位置如下表,己的最高价氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数。下列判断正确的是( )
A.丙与戊的原子序数相差18
B.气态氢化物的稳定性:庚<己<戊
C.常温下,甲和乙的单质均能与水剧烈反应
D.丁的最高价氧化物可用于制造光导纤维
【答案】D
【解析】
己的最高价氧化物对应水化物有强脱水性,则己为S,甲原子最外层与最内层具有相同电子数,则甲为Mg,则结合元素在周期表中的位置可知,甲、乙、丙、丁、戊、己、庚分别为:Mg、Ca、B、Si、As、F,据此解答。
A.戊的原子序数=P的原子序数+18=15+18=33,故丙与戊的原子序数相差:335=28,A错误;
B.由相对位置可知,非金属性:庚>己>戊,故气态氢化物的稳定性:庚>己>戊,B错误;
C.常温下,甲(Mg)与水缓慢反应,C错误;
D.丁为Si,丁的最高价氧化物即SiO2可用于制造光导纤维,D正确。
答案选D。

练习册系列答案
相关题目