题目内容
小苏打、胃舒平、达喜都是常用的中和胃酸的药物。
(1)小苏打片每片含0.50 g NaHCO3,2片小苏打片和胃酸完全中和,被中和的氢离子是___________mol。
(2)胃舒平每片含0.245 g Al(OH)3。中和胃酸时,6片小苏打片相当于胃舒平__________片。
(3)达喜的化学成分是铝和镁的碱式盐。
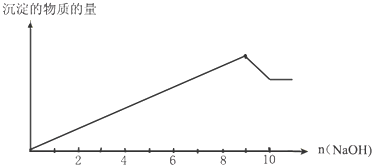
①取该碱式盐3.01 g,加入2.0 mol?L-1盐酸使其溶解,当加入盐酸42.5 mL时开始产生CO2,加入盐酸至45.0 mL 时正好反应完全,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比。
②在上述碱式盐溶于盐酸后的溶液中加入过量氢氧化钠,过滤,沉淀物进行干燥后重1.74 g,若该碱式盐中氢元素的质量分数为0.040,试推测该碱式盐的化学式。
(1)0.012 mol
(2)3.8
(3)n(OH-)∶n(![]() )=16∶1
)=16∶1
(4)Al2Mg6(OH)16CO3?4H2O
解析:(1)被中和的氢离子为n(H+)=0.50 g÷84 g?mol-1×2=0.012 mol
注意保留两位有效数字
(2)设所需胃舒平数量为x
根据题意得关系式:3NaHCO3―3H+―Al(OH)3
3×84 g 78 g
6×0.50 g x?0.245 g
解得:x=3.8
(3)加入的42.5 mL盐酸是完成两个反应:H++OH-![]() H2O H++
H2O H++![]()
![]()
![]()
而后面加入的2.5 mL盐酸是完成反应:![]() +H+
+H+![]() CO2↑+H2O
CO2↑+H2O
所以n(OH-)∶n(![]() )=(42.5-2.5) mol∶2.5 mol=16∶1
)=(42.5-2.5) mol∶2.5 mol=16∶1
其中n(OH-)=(0.042 5 L-0.002 5 L)×2.0 mol?L-1=0.08 mol
n(![]() )=0.005 mol
)=0.005 mol
加入过量NaOH溶液生成的沉淀是Mg(OH)2,其物质的量为1.74 g÷58 g?mol-1=0.03 mol
酸式盐中H元素的质量分数为0.040可得n(H)=3.01 g×0.040÷1 g?mol-1=0.12 mol
则n(H2O)=(0.12 mol-0.08 mol)÷2=0.02 mol
最后得n(Al3+)=0.01 mol
该酸式盐的化学式为 Al2Mg6(OH)16CO3?4H2O