题目内容
铁及铝的化合物有多种作途.请解答下面有关问题:
(1)小苏打、胃舒平、达喜都是常用的中和胃酸(主要成分为盐酸)的药物.
①市售小苏打片每片含0.42gNaHCO3,根据医嘱,某病人一次要服用2片小苏打片,则可中和盐酸
mol.
②若改用胃舒平,要达到同样药效,需胃舒平
③达喜的化学成分是铝和镁的碱式盐,其化学式为:Al2Mg6(OH)16CO3?4H2O.请写出达喜和胃酸反应的化学方程式
(2)Fe2O3可以与铝粉组成铝热剂用于焊接钢轨或定向爆破.某同学猜测,该反应所得熔融物中含有Fe2O3.他设计如下实验来验证自己的猜想:取少量试样,加入足量稀盐酸,然后滴加KSCN溶液,若出现血红色,证明含有Fe2O3.否则,不含有Fe2O3.你认为该方案合理吗?为什么?
(3)用FeCl3溶液溶解铜电路板回收铜,化学反应中被还原的元素名称是
(1)小苏打、胃舒平、达喜都是常用的中和胃酸(主要成分为盐酸)的药物.
①市售小苏打片每片含0.42gNaHCO3,根据医嘱,某病人一次要服用2片小苏打片,则可中和盐酸
0.01
0.01
mol.
②若改用胃舒平,要达到同样药效,需胃舒平
1
1
片.【胃舒平每片含0.260gAl(OH)3】③达喜的化学成分是铝和镁的碱式盐,其化学式为:Al2Mg6(OH)16CO3?4H2O.请写出达喜和胃酸反应的化学方程式
Al2Mg6(OH)16CO3?4H2O+18H+═2Al3++6Mg2++CO2↑+21H2O
Al2Mg6(OH)16CO3?4H2O+18H+═2Al3++6Mg2++CO2↑+21H2O
(2)Fe2O3可以与铝粉组成铝热剂用于焊接钢轨或定向爆破.某同学猜测,该反应所得熔融物中含有Fe2O3.他设计如下实验来验证自己的猜想:取少量试样,加入足量稀盐酸,然后滴加KSCN溶液,若出现血红色,证明含有Fe2O3.否则,不含有Fe2O3.你认为该方案合理吗?为什么?
不合理.因为Fe3+能跟Fe反应生成Fe2+,Fe2+与SCN-反应时不会出现血红色
不合理.因为Fe3+能跟Fe反应生成Fe2+,Fe2+与SCN-反应时不会出现血红色
.(3)用FeCl3溶液溶解铜电路板回收铜,化学反应中被还原的元素名称是
铁
铁
.分析:(1)①根据碳酸氢钠的质量求氯化氢的物质的量;
②根据方程式找出氢氧化铝与碳酸氢钠之间的关系;
③Al2Mg6(OH)16CO3?4H2O与氢离子反应生成铝离子、镁离子和二氧化碳;
(2)熔融物中有铁粉;
(3)化合价降低的物质被还原.
②根据方程式找出氢氧化铝与碳酸氢钠之间的关系;
③Al2Mg6(OH)16CO3?4H2O与氢离子反应生成铝离子、镁离子和二氧化碳;
(2)熔融物中有铁粉;
(3)化合价降低的物质被还原.
解答:解:(1)①设被中和的HCl的物质的量为x
NaHCO3+HCl═NaCl+H2O+CO2↑
84 1
0.42g×2 x
=
x=0.01mol,故答案为:0.01;
②设相当于氢氧化铝的片数为y
由方程式Al(OH)3+3HCl=AlCl3+3H2O和NaHCO3+HCl═NaCl+H2O+CO2↑
得关系式Al(OH)3~3HCl~3NaHCO3
78 3×84
0.260g×y 0.42g×2
=
y=1片
故答案为:1;
③Al2Mg6(OH)16CO3?4H2O与氢离子反应生成铝离子、镁离子和二氧化碳,离子方程式Al2Mg6(OH)16CO3?4H2O+18H+═2Al3++6Mg2++CO2↑+21H2O,
故答案为:Al2Mg6(OH)16CO3?4H2O+18H+═2Al3++6Mg2++CO2↑+21H2O;
(2)熔融物中有铁粉,Fe3+能跟Fe反应生成Fe2+,故答案为:不合理.因为Fe3+能跟Fe反应生成Fe2+,Fe2+与SCN-反应时不会出现血红色;
(3)2FeCl3+Cu═2FeCl2+CuCl2,FeCl3中的铁化合价降低,被还原,故答案为:铁.
NaHCO3+HCl═NaCl+H2O+CO2↑
84 1
0.42g×2 x
| 84 |
| 0.42g×2 |
| 1 |
| x |
x=0.01mol,故答案为:0.01;
②设相当于氢氧化铝的片数为y
由方程式Al(OH)3+3HCl=AlCl3+3H2O和NaHCO3+HCl═NaCl+H2O+CO2↑
得关系式Al(OH)3~3HCl~3NaHCO3
78 3×84
0.260g×y 0.42g×2
| 78 |
| 0.260g×y |
| 3×84 |
| 0.42g×2 |
y=1片
故答案为:1;
③Al2Mg6(OH)16CO3?4H2O与氢离子反应生成铝离子、镁离子和二氧化碳,离子方程式Al2Mg6(OH)16CO3?4H2O+18H+═2Al3++6Mg2++CO2↑+21H2O,
故答案为:Al2Mg6(OH)16CO3?4H2O+18H+═2Al3++6Mg2++CO2↑+21H2O;
(2)熔融物中有铁粉,Fe3+能跟Fe反应生成Fe2+,故答案为:不合理.因为Fe3+能跟Fe反应生成Fe2+,Fe2+与SCN-反应时不会出现血红色;
(3)2FeCl3+Cu═2FeCl2+CuCl2,FeCl3中的铁化合价降低,被还原,故答案为:铁.
点评:本题考查物质的量的计算、二价铁和三价铁的转化和检验,题目难度中等,注意化学方程式的书写是解题的关键.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案
相关题目
(选做题)(19分)图表法、模型法是常用的科学研究方法。
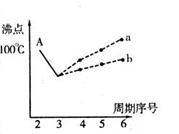
I.下图是研究部分元素的氢化物的沸点变化规律的图像。不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线——折线a和折线b(其中A点对应的沸点是100℃),你认为正确的是 ,理由是 。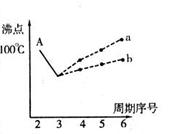
II.人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属则被科学家预测为是钛(Ti)。钛被誉为“未来世纪的金属”。试回答下列问题:
(1)22Ti元素基态原子的价电子层排布式为 。
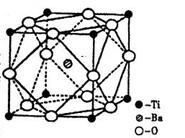
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好,价电常数高,在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构示意图如右图,则它的化学式是 。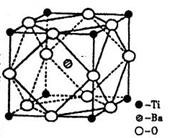
III.上世纪60年化,第一个稀有气体化合物Xe[PtF6]被合成出来后,打破了“绝对情性”的观念。在随后的几年内,科学家又相继后成了氙的氟化物、氧化物等。
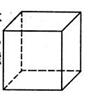
(1)金属Pt内部原子的堆积方式与铜及干冰中的CO2相同,右图正方体是Pt晶胞的示意图,试说出Pt原子在晶胞中的位置 。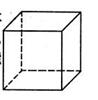
(2)稀有气体(氡除外)中,只有较重的氙能合成出多种化合物,
其可能原因是 (填字母代号)
| A.氙的含量比较丰富 | B.氙的相对原子质量大 |
| C.氙原子半径大,电离能小 | D.氙原子半径小,电负性大 |