题目内容
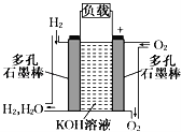
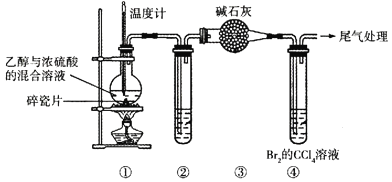
【题目】某小组同学利用图1装置(夹持仪器已省略)制备溴苯,并探究该反应原理。
Ⅰ.制备溴苯
(1)装置中长导管a的作用是__________、导出气体。
(2)本实验所获得的溴苯为褐色,是因为_________.
Ⅱ.分离提纯
已知,溴苯与苯互溶,液溴、苯、溴苯的沸点依次为59℃、80℃、156℃。同学们设计了如图2流程:
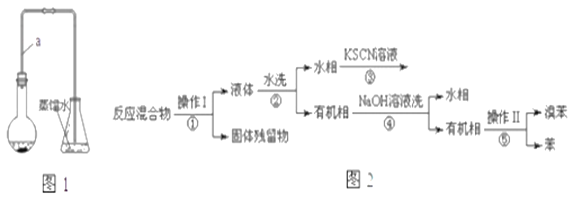
(3)操作Ⅱ为________.
(4)流程②和④中,需要用到的玻璃仪器是烧杯、___;流程③的现象为____,流程④的作用是_____.
Ⅲ.探究原理
(5)反应结束后,某同学取少量锥形瓶中的液体于试管中,再滴入几滴AgNO3溶液,出现浅黄色浑浊,从而判断反应一定生成了HBr,你认为该同学的判断________(填“合理”、“不合理”)。
(6)为探究锥形瓶中溶液的离子,请完成如表探究实验方案(限选试剂:镁粉、四氯化碳、氯水、溴水、蒸馏水)
实验步骤 | 预期现象 | 结论 |
1.将锥形瓶中的液体转入分液漏斗,加足量①__,振荡后分液。分别取少量②_层溶液于试管A、B中 | _______ | ______ |
2.向试管A中加入少量③___和四氯化碳,振荡后静置; | 溶液分层,下层显④___色 | 锥形瓶中液体含大量Br |
3.向试管B中加入⑤___. | 有汽泡生成 | 锥形瓶中液体含大量⑥___ |
根据上述结论推断,制备溴苯的反应属于___反应,其反应方程式为______。
【答案】冷凝回流 溴苯中溶有溴而呈褐色 蒸馏 分液漏斗 溶液变红色 除去溴苯中混有的Br2 不合理 四氯化碳 上 氯水 橙红色 镁粉 H+ 取代反应 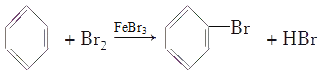
【解析】
(1)根据图1,反应为放热反应,长导管让挥发出来溴单质、苯冷凝,提高原料的利用率,即长导管的作用是冷凝回流、导气;
(2)溴苯是无色液体,溴苯中溶有溴而呈褐色;
(3)反应混合物中含有苯、溴苯、溴、FeBr3以及Fe,由流程可知经操作I后得到固体残留物和液体,则操作I为过滤,固体残留物为Fe,液体中含有FeBr3等,水洗后进行分液分离,有机相含有苯、溴苯、溴,加入NaOH溶液除去Br2,再经过分液分离,水相中主要含有NaBr和NaBrO等,有机相中含有苯、溴苯,由于二者沸点不同,进行蒸馏分离,即操作II为蒸馏;
(4)流程②④得到水相和有机相,应为分液,除需要烧杯外,还需要分液漏斗;流程②分液后的水相溶液中含有Fe3+,流程③滴加KSCN溶液,溶液变红色;流程④的作用是除去溴苯中混有的Br2;
(5)由于溴单质易挥发,锥形瓶中有挥发出来的Br2,Br2也能与AgNO3溶液产生浅黄色沉淀,干扰了HBr的检验,因此该同学判断不合理;
(6)为探究锥形瓶中溶液的离子,根据题给试剂,1.使混合液分层,需要加入有机溶剂,则①为四氯化碳,由于四氯化碳的密度大于水,则含有离子的溶液在上层,有机溶剂在下层,应该取上层溶液,即②为上;
2.根据结论“锥形瓶中含大量Br-”,则③为氧化剂,即氯水将Br-氧化成Br2,CCl4将Br2萃取到CCl4层,则下层④为橙红色;
3.根据实验现象“有气泡生成”,则气泡为H2,⑤应该是加入金属镁粉,证明了溶液中含有大量H+,则锥形瓶中液体含大量⑥H+;
通过实验可知,溶液中存在大量的H+和Br-,从而证明苯与液溴在铁作催化剂下发生取代反应,生成溴苯和HBr,其反应方程式为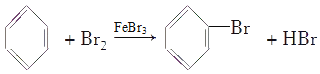 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案