题目内容
【题目】硫酰氯(SO2Cl2)常作氯化剂或氯璜化剂,用于制作药品、染料、表面活性剂等。有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
SO2Cl2 | -54.1 | 69.1 | ①易水解,产生大量白雾②易分解:SO2Cl2 |
H2SO4 | 10.4 | 338 | 具有吸水性且不易分解 |
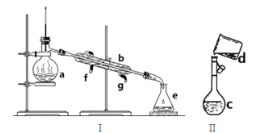
实验室用干燥而纯净的二氧化硫和氯气合成硫酰氯,反应的化学方程式为SO2(g)+Cl2(g) ![]() SO2Cl2(l)△H=-97.3kJ/mol。装置如图所示(夹持仪器已省略),请回答有关问题:
SO2Cl2(l)△H=-97.3kJ/mol。装置如图所示(夹持仪器已省略),请回答有关问题:
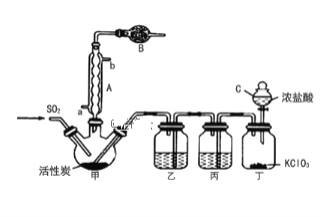
(1)仪器B的名称是______,作用是________。
(2)若无装置乙硫酰氯会发生水解,则硫酰氯水解反应的化学方程式为_______。
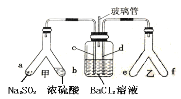
(3)写出丁装置中发生反应的化学反应方程式____________。
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有____(填序号)。
①先通冷凝水,再通气 ②控制气流速率,宜慢不宜快③若三颈烧瓶发烫,可适当降温④加热三颈烧瓶
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为______。此方法得到的产品中会混有硫酸,从分解产物中分离出硫酰氯的方法是_____。
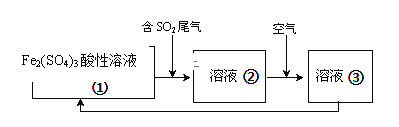
(6)工业上处理SO2废气的方法很多,例如可以用Fe2(SO4)3酸性溶液处理,其工艺流程如下,溶液②转化为溶液③发生反应的离子方程式为_________。
【答案】干燥管 吸收未反应完的氯气和二氧化硫,防止污染空气;防止空气中水蒸气进人甲,防止SO2Cl2水解 SO2Cl2+2H2O═H2SO4+2HCl KClO3+6HCl=KCl+3Cl2+3H2O ①②③ 2ClSO3H=H2SO4+SO2Cl2 蒸馏 4H++4Fe2++O2=4Fe3++2H2O
【解析】
(1)根据装置图判断仪器B的名称,根据SO2Cl2易水解回答;
(2)SO2Cl2水解为盐酸和硫酸;
(3)丁装置中氯酸钾与浓盐酸反应制备氯气;
(4)根据影响反应速率的因素、平衡移动原理分析;
(5)根据元素守恒,氯磺酸(ClSO3H)分解生成SO2Cl2和硫酸;
(6)溶液②中的Fe2+被氧气氧化为Fe3+;
(1)根据装置图,仪器B的名称是干燥管;氯气和二氧化硫有毒,能被碱性物质吸收,SO2Cl2易水解,所以装置B的作用是吸收未反应完的氯气和二氧化硫,防止污染空气;防止空气中水蒸气进人甲,防止SO2Cl2水解;
(2)SO2Cl2水解为盐酸和硫酸,水解方程式是SO2Cl2+2H2O═H2SO4+2HCl;
(3)丁装置中氯酸钾与浓盐酸反应制备氯气;发生反应的化学反应方程式是KClO3+6HCl=KCl+3Cl2+3H2O;
(4)①正反应放热,降低温度有利于平衡正向移动,先通冷凝水,再通气,能提高SO2Cl2的产率,故选①;
②控制气流速率,宜慢不宜快,能使反应充分,有利于提高SO2Cl2的产率,故选②;
③正反应放热,适当降温,使平衡正向移动,能提高SO2Cl2的产率,故选③;
④正反应放热,加热三颈烧瓶,平衡逆向移动, SO2Cl2的产率降低,故不选④;
(5)氯磺酸(ClSO3H)分解生成SO2Cl2和硫酸,反应方程式是2ClSO3H=H2SO4+SO2Cl2;硫酰氯与硫酸的沸点不同,可用蒸馏法分离出硫酰氯;
(6)溶液②中的Fe2+被氧气氧化为Fe3+,反应的离子方程式是4H++4Fe2++O2=4Fe3++2H2O;

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】(1)填写下列表格:
物质 | 分子数 | 质量/g | 物质的量/ mol | 摩尔质量/(g |
O2 | __ | 8.0 | __ | __ |
H2SO4 | 3.01×1023 | __ | __ | __ |
H2O | __ | __ | 0.5 | __ |
(2)147gH2SO4的物质的量是____;0.5molH2SO4的质量是____g,其中含有____mol H;2 mol H2SO4中含有H2SO4分子数为_____个,含氢原子数为____个。
(3)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为____,R的相对原子质量为____。含R的质量为1.6 g的Na2R,其物质的量为____。