题目内容
对如图所示的实验装置的判断中错误的是 
| A.若X为碳棒,开关K置于A处可减缓铁的腐蚀 |
| B.若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀 |
| C.若X为锌棒,开关K置于B处时,为牺牲阳极的阴极保护法 |
| D.若X为碳棒,开关K置于B处时, |
D
解析试题分析:若开关K置于A处时,装置形成电解池,其中X为阳极,Fe为阴极,阴极被保护,可减缓铁的腐蚀,所以A正确,方程式为NaCl + H2O 电解 H2↑+ Cl2↑+ NaOH,若将开关置于B处时,装置形成原电池,当X为锌棒时,X为正极,Fe为负极,正极被保护,为牺牲阳极的阴极保护法,可减缓铁的腐蚀,所以B、C正确;当X\为碳棒时,X为正极,Fe为负极,负极:Fe - 2e- = Fe2+,正极:O2 + 2H2O + 4e- = 4OH-故选D。
考点:考查电解池、原电池

 智能训练练测考系列答案
智能训练练测考系列答案关于下图所示装置(盐桥含KCl)的叙述,正确的是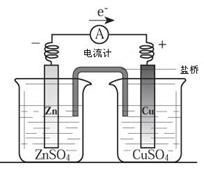
| A.铜离子在铜片表面被氧化 |
| B.铜作阳极,铜片上有气泡产生 |
| C.电流从锌片经导线流向铜片 |
| D.右侧烧杯中,SO42-的物质的量几乎不变,K+的数目增多 |
浙江大学的科研小组成功研制出能在“数分钟之内”将电量充满的锂电池,其成本只有传统锂电池的一半。他们把锂锰氧化物(LMO)浸泡在石墨里面,使其变成一个可以导电的密集网络的负极材料(如图),与电解质和正极材料(石墨)
构成可充电电池。若电解液为LiAlCl4-SOCl2,电池的总反应为:
4LiCl+S+SO2 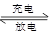 4Li+2SOCl2。下列说法正确的是( )
4Li+2SOCl2。下列说法正确的是( )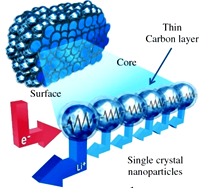
| A.电池的电解液可为LiCl水溶液 |
| B.该电池放电时,负极发生还原反应 |
| C.充电时阳极反应式为:4Cl-+S+SO2-4e-=2SOCl2 |
| D.放电时电子从负极经外电路流向正极,再从正极经电解质流向负极 |
下列关于原电池的叙述中,正确的是( )
| A.把电能转化为化学能,使溶液发生氧化还原反应 |
| B.电子从活泼金属流向不活泼金属,不活泼金属为负极 |
| C.外电路中电子从负极流向正极 |
| D.正极发生氧化反应 |
下图所示的电解池I和II中,a、b、c和d均为Pt电极。电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d。符合上述实验结果的盐溶液是
| 选项 | X | Y |
| A. | MgSO4 | CuSO4 |
| B. | AgNO3 | Pb(NO3)2 |
| C. | FeSO4 | Al2 (SO4)3 |
| D. | CuSO4 | AgNO3 |
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
| A.两烧杯中铜片表面均无气泡产生 | B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 | D.产生气泡的速度甲比乙慢 |
锌溴液流电池是一种新型电化学储能装置(如右图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是
| A.充电时电极a连接电源的负极 |
| B.放电时负极的电极反应式为Zn—2e-=Zn2+ |
| C.放电时左侧电解质储罐中的离子总浓度增大 |
| D.阳离子交换膜可阻止Br2与Zn直接发生反应 |
用铅蓄电池电解甲、乙电解池中的溶液。 电解一段时间后向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是( ) 
| A.d极为阴极 |
| B.若利用甲池精炼铜,b极应为粗铜 |
| C.放电时铅蓄电池负极的电极反应式为: PbO2(s) + 4 H+(aq)+SO4 2-(aq)+4e- = PbSO4 (s) +2H2O (l) |
| D.若四个电极材料均为石墨,当析出6.4 g Cu时,两池中共产生气体3.36 L(标准状况下) |
