题目内容
【题目】肼(分子式为N2H4,又称联氨)具有可燃性,在氧气中完全燃烧生成氮气,可用作燃料电池的燃料。由题图信息可知下列叙述不正确的是( )
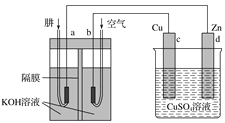
甲 乙
A. 甲为原电池,乙为电解池
B. b电极的电极反应式为O2+4e-=2O2-
C. d电极的电极反应式为Cu2++2e-=Cu
D. c电极质量变化128 g时,理论消耗标准状况下的空气约为112 L
【答案】B
【解析】
A.甲是燃料电池,把化学能转化为电能,作原电池,乙是电解池,故A正确;
B.正极上是氧气发生得电子的还原反应,在碱性环境下,电极反应式为:2H2O+O2+4e-=4OH-,故B错误;
C.锌与电源负极相连,是电解池的阴极,在该电极上铜离子得到电子生成铜,故电极反应式为Cu2++2e-=Cu,故C正确;
D. 电解硫酸铜溶液时,铜电极上铜失电子发生氧化反应,当铜片的质量变化128g,失去电子的物质的量=2×![]() =4mol,1mol氧气生成-2价氧元素得到4mol电子,则需要空气的体积=1mol × 22.4L/ mol÷20%=112L,故D正确;
=4mol,1mol氧气生成-2价氧元素得到4mol电子,则需要空气的体积=1mol × 22.4L/ mol÷20%=112L,故D正确;
故选B。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目