题目内容
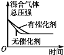
【题目】氮、磷属于同一主族元素,是组成生命体的重要元素,其单质及化合物用途广泛。回答下列问题:
(1)基态P原子的核外电子排布式为___________________
(2)自然固氮现象发生的一系列化学变化:![]() ,解释了民谚“雷雨发庄稼”的原理。
,解释了民谚“雷雨发庄稼”的原理。
①![]() 分子结构中σ键和π键数目之比为__________
分子结构中σ键和π键数目之比为__________
②![]() 中N原子采取__________杂化方式,写出它的一种等电子体的化学式:__________。
中N原子采取__________杂化方式,写出它的一种等电子体的化学式:__________。
③已知酸性:![]() ,下列相关见解合理的是__________。
,下列相关见解合理的是__________。
A.含氧酸中氧原子总数越多,酸性越强
B.同种元素化合价越高,对应含氧酸的酸性越强
C.![]() 中氮元素的正电性更高,在水溶液中更易电离出
中氮元素的正电性更高,在水溶液中更易电离出![]() ,酸性强于
,酸性强于![]()
(3)磷化硼(BP)是一种超硬耐磨涂层材料,其晶胞结构如图所示,图中a点和b点的原子坐标参数分别为(0,0,0)、![]() ,则c点的原子坐标参数为__________。已知该晶体密度为
,则c点的原子坐标参数为__________。已知该晶体密度为![]() ,则B—P键的键长为__________pm(阿伏加德罗常数用
,则B—P键的键长为__________pm(阿伏加德罗常数用![]() 表示,列出计算式即可)。
表示,列出计算式即可)。
 。
。
【答案】![]() 1∶2 sp2 SO3或O4或BF3等 BC
1∶2 sp2 SO3或O4或BF3等 BC ![]()
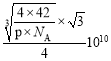
【解析】
(1).P元素的原子序数为15,核外电子为3层,有5个能级;
(2)①N2分子中含有氮氮三键,结构式为N≡N,氮氮三键由一个σ键和两个π键形成;
②硝酸根中N原子价电子层电子对数为3,孤电子对数为0,杂化方式为sp2杂化;原子个数和价电子数相同的微粒互为等电子体;
③同种元素化合价越高,含氧酸中氧原子总数越多,非羟基氧原子个数越多,正电性更高,在水溶液中更易电离出![]() ,酸性越强;
,酸性越强;
(3)由a、b的坐标可知晶胞的边长为1,由晶胞结构可知c位于右侧面的面心,则c的坐标为(1, ![]() ,
, ![]() );由分摊法计算可得。
);由分摊法计算可得。
(1).P元素的原子序数为15,核外电子为3层,有5个能级,电子排布式为1s22s22p63s23p3,故答案为:1s22s22p63s23p3;
(2)①N2分子中含有氮氮三键,结构式为N≡N,氮氮三键由一个σ键和两个π键形成,则σ键和π键之比为1:2,故答案为:1:2;
②硝酸根中N原子价电子层电子对数为3,孤电子对数为0,则杂化方式为sp2杂化;原子个数和价电子数相同的微粒互为等电子体,则与硝酸根互为等电子体的微粒为SO3或O4或BF3等,故答案为:SO3或O4或BF3等;
③A.含氧酸中非羟基氧原子个数越多,酸性越强,与氧原子总数无关,故错误;
B.同种元素化合价越高,含氧酸中氧原子总数越多,非羟基氧原子个数越多,酸性越强,故正确;
C. HNO3中氮元素的化合价高,正电性更高,在水溶液中更易电离出![]() ,所以相较HNO2酸性更强,故正确;
,所以相较HNO2酸性更强,故正确;
BC正确,故答案为:BC;
(3)由a、b的坐标可知晶胞的边长为1,由晶胞结构可知c位于右侧面的面心,则c的坐标为(1, ![]() ,
, ![]() );由晶胞结构可知,b处于4个P原子围成的正方体的正中心,P原子位于顶点,设x为晶胞边长,则B-P键的长度为
);由晶胞结构可知,b处于4个P原子围成的正方体的正中心,P原子位于顶点,设x为晶胞边长,则B-P键的长度为![]() ;由晶胞结构可知,晶胞中含有4个BP ,由
;由晶胞结构可知,晶胞中含有4个BP ,由![]() =x3ρ可得x=
=x3ρ可得x=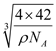 ,则B-P键长为
,则B-P键长为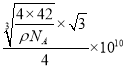 pm,故答案为:(1,
pm,故答案为:(1, ![]() ,
, ![]() );
); 。
。
![]()

 世纪百通期末金卷系列答案
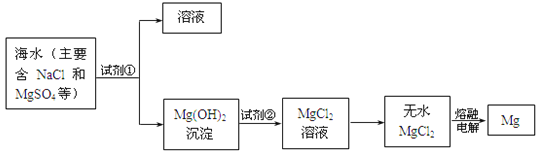
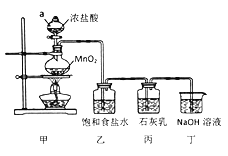
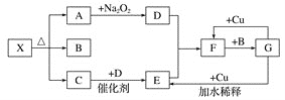
世纪百通期末金卷系列答案【题目】(I)如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置。请根据该装置回答下列问题:
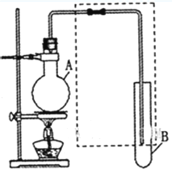
(1)若用乙醇与乙酸反应制取乙酸乙酯,则烧瓶A中加入的试剂在混合时的操作方法是___________,反应的化学方程式为___________,试管B中应加入___________。虚线框中的导管除用于导气外,还兼有___________作用。
(2)若用该装置分离乙酸和1-丙醇,则在烧瓶A中除加入1-丙醇与乙酸外,还应先加入适量的试剂___________,加热到一定温度,试管B中收集到的是(填写化学式)___________。冷却后,再向烧瓶中加入试剂___________再加热到一定温度,试管B中收集到的是___________(填写化学式)。
(3)若用该装置(不用加热)证明酸性:醋酸>碳酸>苯酚,则在烧瓶A中加入___________,试管B中应加入___________。
(II)正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛,发生:CH3CH2CH2CH2OH→![]() CH3CH2CH2CHO。
CH3CH2CH2CHO。
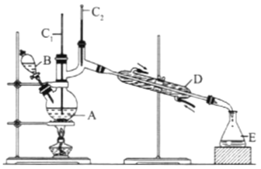
反应物和产物的相关数据列表:
沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
正丁醇 | 11.72 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
实验步骤如下:
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90-95℃,在E中收集90℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75-77℃馏分,产量2.0g。
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由:__________。
(2)加入沸石的作用是__________;若加热后发现未加沸石,应采取的正确方法是__________。
(3)上述装置图中,B仪器的名称是__________,D仪器的名称是__________。
(4)分液漏斗使用前必须进行的操作是(填字母)__________。
A.润湿 B.干燥 C.检漏 D.标定
(5)将正丁醛粗产品置于分液漏斗中分液时,水在__________层(填“上”,或“下”)。
(6)反应温度应保持在90~95℃,其原因是__________。
(7)本实验中,正丁醛的产率为__________%。.
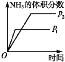
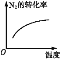
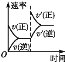
【题目】对于可逆反应N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,下列研究目的和示意图相符的是( )
2NH3(g) ΔH<0,下列研究目的和示意图相符的是( )
A | B | C | D | |
研究目的 | 压强对反应的影响(p2>p1) | 温度对反应的影响 | 平衡体系中增加N2的浓度对反应的影响 | 催化剂对反应的影响 |
示意图 |
|
|
|
|
A. AB. BC. CD. D