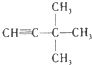
��Ŀ����
����Ŀ��þ����Ͻ�����;�ܹ�Ľ������ϣ�Ŀǰ������60%��þ�ǴӺ�ˮ����ȡ�ġ���Ҫ�������£�
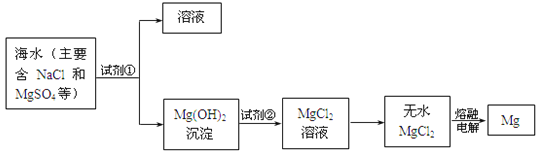
��1��Ϊ��ʹMgSO4ת��ΪMg(OH)2���Լ��ٿ���ѡ��_________��
��2����ˮMgCl2������״̬�£�ͨ������þ���������÷�Ӧ�Ļ�ѧ����ʽΪ__________________��
��3����������ĸ��������������ڹ�ҵ��Ư�ۡ�ij��ȤС��ģ�ҵ��Ư�ۣ��������ͼ��ʵ��װ�á�
��֪���������ͼӦ�ų���������6Cl2+6Ca(OH)2![]() 5CaCl2+Ca(ClO3)2+6H2O
5CaCl2+Ca(ClO3)2+6H2O
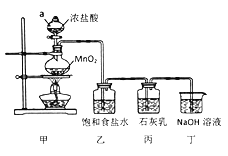
�ش��������⣺
�ټ�װ��������a��������____________________��
��װ�����б���ʳ��ˮ��������__________________________________��
����ȡƯ�۵Ļ�ѧ����ʽ��_____________________________________��
�ܸ�С���Ƶõ�Ư����n(CaCl2)Զ����n(Ca(ClO)2]������Ҫԭ����_________��
��Ϊ��߱���Ca(ClO)2�ĺ������ɲ�ȡ�Ĵ�ʩ��_______________(��дһ�ּ���)��
���𰸡� NaOH��Һ MgCl2(����)![]() Mg+Cl2�� ��Һ©�� ��ȥ�����л��е��Ȼ��� 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O �����ͼӦ��ų������������¶����ߣ������˸���Ӧ��6Cl2+6Ca(OH)2
Mg+Cl2�� ��Һ©�� ��ȥ�����л��е��Ȼ��� 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O �����ͼӦ��ų������������¶����ߣ������˸���Ӧ��6Cl2+6Ca(OH)2![]() 5CaCl2+Ca(ClO3)2+6H2O(����������Ҳ����) ����װ�ý���ʢ����ˮ��ˮ���л����������������(����������Ҳ����)
5CaCl2+Ca(ClO3)2+6H2O(����������Ҳ����) ����װ�ý���ʢ����ˮ��ˮ���л����������������(����������Ҳ����)
����������1��Ϊ��ʹMgSO4ת��ΪMg(OH)2��Ӧ��ѡ�ü�Һ�������Լ��ٿ���ѡ��NaOH��Һ����2����ˮMgCl2������״̬�£�ͨ������þ���������÷�Ӧ�Ļ�ѧ����ʽΪMgCl2(����)![]() Mg+Cl2������3���ټ�װ��������a�������Ƿ�Һ©�����ڷ�Ӧ���ɵ������к����Ȼ��⣬�Ȼ�������ʯ���鷴Ӧ����Ҫ��ȥ�������Ȼ��⼫������ˮ������װ�����б���ʳ��ˮ�������dz�ȥ�����л��е��Ȼ��⣻����ȡƯ�۵Ļ�ѧ����ʽ��2Cl2+2Ca(OH)2��CaCl2+Ca(ClO)2+2H2O�������������ͼӦ��ų������������¶����ߣ������˸���Ӧ��6Cl2+6Ca(OH)2
Mg+Cl2������3���ټ�װ��������a�������Ƿ�Һ©�����ڷ�Ӧ���ɵ������к����Ȼ��⣬�Ȼ�������ʯ���鷴Ӧ����Ҫ��ȥ�������Ȼ��⼫������ˮ������װ�����б���ʳ��ˮ�������dz�ȥ�����л��е��Ȼ��⣻����ȡƯ�۵Ļ�ѧ����ʽ��2Cl2+2Ca(OH)2��CaCl2+Ca(ClO)2+2H2O�������������ͼӦ��ų������������¶����ߣ������˸���Ӧ��6Cl2+6Ca(OH)2![]() 5CaCl2+Ca(ClO3)2+6H2O����˵����Ƶõ�Ư����n(CaCl2)Զ����n(Ca(ClO)2]����Ϊ��߱���Ca(ClO)2�ĺ�������Ҫ���⸱��Ӧ���������Ҫ��취�����¶ȣ����Կɲ�ȡ�Ĵ�ʩ�ǽ���װ�ý���ʢ����ˮ��ˮ���л���������������ʡ�
5CaCl2+Ca(ClO3)2+6H2O����˵����Ƶõ�Ư����n(CaCl2)Զ����n(Ca(ClO)2]����Ϊ��߱���Ca(ClO)2�ĺ�������Ҫ���⸱��Ӧ���������Ҫ��취�����¶ȣ����Կɲ�ȡ�Ĵ�ʩ�ǽ���װ�ý���ʢ����ˮ��ˮ���л���������������ʡ�

����Ŀ�����ס���Ԫ�صĵ��ʺͻ�����Ӧ�ù㷺��
��1����Ԫ�ص�ԭ�ӽṹʾ��ͼ�� ��
��2��������뽹̿��ʯӢɰ��ϣ��ڵ�¯�м��ȵ�1500�����ɰ��ף���ӦΪ��
2Ca3��PO4��2+6SiO2�T6CaSiO3+P4O10 10C+P4O10�TP4+10CO
ÿ����1mol P4ʱ������mol���ӷ���ת�ƣ�
��3����������ƣ�Na2S2O3���dz��õĻ�ԭ������ά����C����ѧʽC6H8O6����ˮ��Һ�м������I2��Һ��ʹά����C��ȫ������ʣ���I2��Na2S2O3��Һ�ζ����ɲⶨ��Һ��ά����C�ĺ����������ķ�ӦΪ��
C6H8O6+I2�TC6H6O6+2H++2I�� 2S2O32��+I2�TS4O62��+2I��
��һ�������ijά����C��Һ�м���a molL��1I2��ҺV1mL����ַ�Ӧ����Na2S2O3��Һ�ζ�ʣ���I2 �� ����b molL��1Na2S2O3��ҺV2mL������Һ��ά����C�����ʵ�����mol��
��4����������Һ�У�����أ�KIO3�����������ƿɷ������·�Ӧ��2IO3��+5SO32��+2H+�TI2+5SO42��+H2O���ɵĵ�����õ�����Һ���飬���ݷ�Ӧ��Һ������ɫ�����ʱ���������÷�Ӧ�����ʣ�ijͬѧ���ʵ�������ʾ��
0.01molL��1 | 0.01molL��1 | H2O����� | ʵ�� | ��Һ������ɫʱ����ʱ��/s | |
ʵ��1 | 5 | V1 | 35 | 25 | |
ʵ��2 | 5 | 5 | 40 | 25 | |
ʵ��3 | 5 | 5 | V2 | 0 |
��ʵ���Ŀ����������V2=mL
��5����ϡ��Ԫ���DZ����ս����Դ���ҹ����̲�����������λ��
�棨Ce���ǵؿ��к�����ߵ�ϡ��Ԫ�أ��ڼ���������CeCl3����ˮ�⣬��ˮCeCl3���ü���CeCl36H2O��NH4Cl��������ķ������Ʊ�������NH4Cl�������� ��
��6����ijǿ���Ի��ϡ����Һ�м���H2O2 �� ����pH��3��Ce3+ͨ�����з�Ӧ�γ�Ce��OH��4�������Է��룮��ɷ�Ӧ�����ӷ���ʽ��Ce3++H2O2+H2O�TCe��OH��4��+ ��
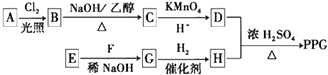
����Ŀ���ں�����ߺ�DZˮͧ�п��ù�������������������ѡ���ʵ��Ļ�ѧ�Լ���ʵ����Ʒ������ͼ�е�ʵ��װ�ý���ʵ�飬֤���������ƿ�����������
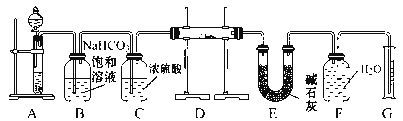
��1��A����ȡCO2��װ�á�д��A�з�����Ӧ�Ļ�ѧ����ʽ��____________________��
��2��B��C��E��Ϊ����װ�ã�U���мӹ�������������˳�������
���� | �����Լ� | ������Լ���Ŀ�� |
B | ����NaHCO3��Һ | _________ |
C | Ũ���� | _________ |
E | ��ʯ�� | _________ |
��3��д��B�з�����Ӧ�����ӷ���ʽ��__________________________________��
��4��д��D�й��������������̼��Ӧ�Ļ�ѧ����ʽ��__________________��
��5���Թ�F���ռ��������֤���Թ����ռ���������������ʵ������ǣ�_____��