题目内容
19. 乙醇(C2H5OH)是一种重要的有机物.
乙醇(C2H5OH)是一种重要的有机物.(1)根据乙醇分子式和可能结构推测,1mol乙醇与足量钠反应,产生氢气的物质的量可能是0.5、2.5、3 mol.事实证明反应的乙醇与产生的氢气物质的量比值是2,该反应的化学方程式是2C2H5OH+2Na→2C2H5ONa+H2↑.
(2)乙醇分子中的官能团是羟基.
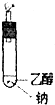
(3)用如图装置实验,干冷烧杯罩在火焰上,有无色液体产生.能否据此说明一定有氢气产生,判断及简述理由是不能,因为氢气中会含有乙醇.
(4)乙醇与钠反应比水与钠反应平缓的多,原因是乙醇中羟基的氢原子比水中氢原子活泼性弱.
分析 (1)依据乙醇结构简式:CH3CH2OH,可知乙醇分子内有两种不同环境下的氢原子,分别是乙基上的氢原子和羟基上的氢原子,据此计算产生氢气的量,判断乙醇的结构,写出方程式;
(2)羟基是乙醇的官能团;
(3)乙醇易挥发,乙醇、氢气燃烧都能生成水;
(4)与水相比较,乙醇的-O-H难以断裂.
解答 解:(1)依据乙醇结构简式:CH3CH2OH,可知乙醇分子内有三种不同环境下的氢原子,如果钠置换的是羟基氢原子,则1mol乙醇与足量钠反应生成0.5mol氢气,如果那置换的是乙基上的氢原子,则1mol乙醇与足量钠反应生成2.5mol氢气,如果乙醇中的氢原子都能够被钠置换,则1mol乙醇与足量钠反应生成3mol氢气,
事实证明反应的乙醇与产生的氢气物质的量比值是2,说明钠与乙醇反应置换的是羟基上的氢原子,所以方程式:2C2H5OH+2Na→2C2H5ONa+H2↑;
故答案为:0.5、2.5、3;2C2H5OH+2Na→2C2H5ONa+H2↑;
(2)乙醇分子中的官能团是羟基,故答案为:羟基;
(3)乙醇易挥发,乙醇、氢气燃烧都能生成水,所以不能据此说明一定有氢气产生;
故答案为:不能,因为氢气中会含有乙醇;
(4)与水相比较,乙醇的-O-H难以断裂,所以乙醇与钠反应比水与钠反应平缓的多,
故答案为:乙醇中羟基的氢原子比水中氢原子活泼性弱.
点评 本题考查了物质的性质,熟悉乙醇的结构及性质是解题关键,题目难度不大.

练习册系列答案
相关题目
9.下列有关氯气的叙述中,正确的是( )
| A. | 工业上常用MnO2和浓盐酸共热来制取氯气 | |
| B. | 新制氯水可使蓝色石蕊试纸先变红后褪色 | |
| C. | 在氧化还原反应中,Cl2只能作氧化剂 | |
| D. | 若提供含0.4 mol HCl的浓盐酸,MnO2过量,则可制得标准状况下氯气2.24 L |
10.下列实验装置所示的实验不能达到实验目的是( )
| A. | 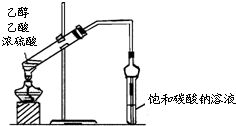 实验室制取乙酸乙酯 | B. | 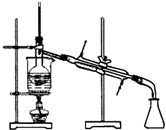 实验室蒸馏石油 | ||
| C. | 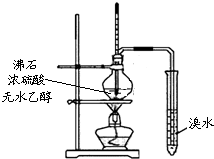 实验室制取乙烯并验证其性质 | D. | 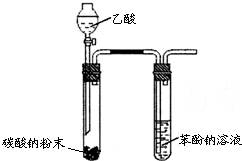 验证乙酸、碳酸、苯酚酸性强弱 |
7.下列物质进行一氯取代反应,产物只有两种的是( )
| A. | (CH3)2CHCH2CH2CH3 | B. | (CH3CH2)2CHCH3 | C. | (CH3)2CHCH(CH3)2 | D. | (CH3)3CCH2CH3 |
14.实验室常用锌片与稀H2SO4反应制取H2.下列措施中能使生成H2的速率加快的是( )
| A. | 向试管内加入水 | |
| B. | 将1mol/L的H2SO4溶液改为1.5mol/L的盐酸 | |
| C. | 将锌片改为锌粉 | |
| D. | 向试管内加少量K2SO4溶液 |
4.2008年9月国家有关部门检出了以三鹿婴幼儿奶粉为首的一批奶制品中掺和的三聚氰胺,并立即对全国的这些奶制品加以封存或销毁.三聚氰胺本是一种优良的化工原料,主要用来制涂料和黏合剂,它的相对分子质量介于100与200之间,碳的质量分数为28.57%,碳、氢的质量比为6:1,其余为氮.则三聚氰胺的分子式为( )
| A. | (CH2N2)n | B. | C3H4ON5 | C. | C3H6N6 | D. | C4H4N5 |
11.氯化硼BCl3的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是( )
| A. | 氯化硼液态时能导电而固态时不导电 | |
| B. | 氯化硼中心原子采用sp杂化 | |
| C. | 三氯化硼遇水蒸气会产生白雾 | |
| D. | 氯化硼分子呈平面正三角形,属非极性分子 |
8.下列鉴别方法不可行的是( )
| A. | 用水鉴别乙醇、甲苯和溴苯 | |
| B. | 用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 | |
| C. | 用燃烧法鉴别乙醇、苯和四氯化碳 | |
| D. | 用酸性高锰酸钾溶液鉴别甲苯、环己烷和环己烯 |
9.下列各组物质中,一定互为同系物的是( )
| A. | HCHO和CH3COOH | B. | CH3COOH和C3H6O2 | C. | C2H4O2 和C4H8O2 | D. | 乙苯和异丙基苯 |