题目内容
14.实验室常用锌片与稀H2SO4反应制取H2.下列措施中能使生成H2的速率加快的是( )| A. | 向试管内加入水 | |
| B. | 将1mol/L的H2SO4溶液改为1.5mol/L的盐酸 | |
| C. | 将锌片改为锌粉 | |
| D. | 向试管内加少量K2SO4溶液 |
分析 增大锌片与稀硫酸的反应速率,可从影响反应速率的外界因素思考,可增大浓度、升高温度、增大固体的表面积以及形成原电池反应等.
解答 解:A.向试管内加入水,减小硫酸浓度,反应速率减慢,故A错误;
B.将1mol/L的H2SO4溶液改为1.5mol/L的盐酸,氢离子浓度在减小,反应速率减慢,故B错误;
C.锌片改为锌粉,固体的表面积增大,反应速率增大,故C正确;
D.加少量K2SO4溶液,减小硫酸浓度,反应速率减慢,故D错误.
故选C.
点评 本题较简单,考查影响化学反应速率的常见因素,为高频考点,侧重于学生的分析能力和基础知识的综合理解和运用的考查,学生应熟悉温度、浓度、构成原电池、增大接触面等对化学反应速率的影响来解答,但浓硫酸的性质是学生解答中容易忽略的知识.

练习册系列答案
相关题目
5.下列各组顺序的排列不正确的是( )
| A. | 熔点:SiO2>CsCl>CCl4>CF4 | |
| B. | 离子半径:F->O2->Al3+>Na+ | |
| C. | 酸性强弱:H2SiO3<H2CO3<H2SO3<HNO3 | |
| D. | 碱性强弱:KOH>NaOH>Mg(OH)2>Al(OH)3 |
2.在玻璃中加入溴化银(AgBr)和氧化铜可制得变色镜片,其中所含物质及变色原理如图所示,下列说法不正确的是( )


| A. | 溴化银应避光保存 | |
| B. | 变色镜片可反复变色 | |
| C. | 变色镜片颜色变深的过程发生了化合反应 | |
| D. | 变色镜片中的氧化铜在变色过程中质量不变 |
9.某核电站的泄漏物质中含有碘-131(${\;}_{54}^{131}$I).${\;}_{54}^{131}$I核内的中子数是( )
| A. | 54 | B. | 77 | C. | 131 | D. | 185 |
6. 2010年11月12日至27日,中国广州成功举办了第16届亚运会,中国代表团共获得了199枚金牌.为保证比赛成绩的公正、公平,反兴奋剂是一项重要而艰巨的工作.某种兴奋剂的结构简式如图所示.有关该物质的说法错误的是( )
2010年11月12日至27日,中国广州成功举办了第16届亚运会,中国代表团共获得了199枚金牌.为保证比赛成绩的公正、公平,反兴奋剂是一项重要而艰巨的工作.某种兴奋剂的结构简式如图所示.有关该物质的说法错误的是( )
 2010年11月12日至27日,中国广州成功举办了第16届亚运会,中国代表团共获得了199枚金牌.为保证比赛成绩的公正、公平,反兴奋剂是一项重要而艰巨的工作.某种兴奋剂的结构简式如图所示.有关该物质的说法错误的是( )
2010年11月12日至27日,中国广州成功举办了第16届亚运会,中国代表团共获得了199枚金牌.为保证比赛成绩的公正、公平,反兴奋剂是一项重要而艰巨的工作.某种兴奋剂的结构简式如图所示.有关该物质的说法错误的是( )| A. | 该有机物能与FeCl3溶液发生显色反应 | |
| B. | 一定条件下1mol该物质能与7molH2发生加成反应 | |
| C. | 该有机物分子中所有的原子不可能在同一平面 | |
| D. | 该有机物是苯酚的同系物 |
3.C6H12和C2H6O的混合物中氧的质量分数为8%,则混合物中氢的质量分数为( )
| A. | 8% | B. | 13% | C. | 14% | D. | 78% |
4.下列化学用语使用不正确的是( )
| A. | Na+的结构示意图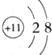 | |
| B. | 聚乙烯的结构简式为CH2=CH2 | |
| C. | 纯碱的化学式为Na2CO3 | |
| D. | 高氯酸(HClO4)中氯元素的化合价为+7 |
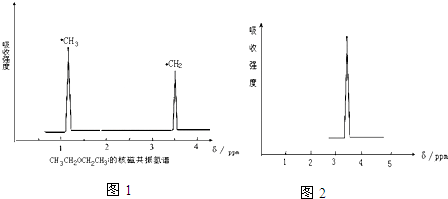
 .
. 乙醇(C2H5OH)是一种重要的有机物.
乙醇(C2H5OH)是一种重要的有机物.