题目内容
5.反应2SO2+O2?2SO3过程中的能量变化曲线如图所示,下列说法中正确的是( )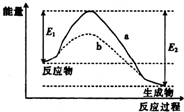
| A. | 由图可知,SO2和O2的总能量一定高于SO3的能量 | |
| B. | 使用正催化剂,E1数值减小 | |
| C. | 曲线b相对曲线a,改变的条件可能是升高温度 | |
| D. | 因该反应为放热反应,故该反应不需要加热 |
分析 A.图象分析反应物能量高于生成物能量;
B.正催化剂降低反应物的活化能;
C.曲线b相对曲线a仅仅是反应物的活化能变大;
D.放热反应与反应条件无关.
解答 解:A.图象分析反应物能量高于生成物能量,但不能判断SO2和O2的总能量一定高于SO3的能量,故A错误;
B.正催化剂降低反应物的活化能,所以使用正催化剂,E1数值减小,故B正确;
C.曲线b相对曲线a仅仅是反应物的活化能变大,而改变的条件为不使用催化剂,不是升高温度,故C错误;
D.放热反应与反应条件无关,燃烧的发热反应就要加热,故D错误.
故选:B.
点评 本题考查了化学变化过程中能量变化的分析的,主要是活化能概念的理解应用,掌握图象分析方法是关键,题目较简单.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
16.下列关于某些有机物的叙述正确的是( )
| A. | 醋酸和蔗糖都是电解质 | |
| B. | 甘氨酸能和盐酸发生化学反应 | |
| C. | 甲烷、乙烯和苯均可使酸性KMnO4溶液褪色 | |
| D. | 乙酸乙酯和植物油均可水解生成乙醇 |
13.下列关于C2H4描述中,正确的是( )
| A. | 含有极性键和非极性键 | B. | 分子为直线形分子 | ||
| C. | 6个原子不在同一平面上 | D. | 有4个σ键和1个π键 |
20.常温下,1mol化学键分解成气态原子所需要的能量用E表示.、结合表中信息判断下列说法不正确的是( )
| 共价键 | H-H | F-F | H-F | H-Cl | H-I |
| E(kJ•mol-1) | 436 | 157 | 568 | 432 | 298 |
| A. | 432kJ•mol-1>E(H-Br)>298kJ•mol-1 | B. | 表中最稳定的共价键是H-F键 | ||
| C. | H2(g)→2H(g)△H=+436kJ•mol-1 | D. | H2(g)+F2(g)=2HF(g)△H=-25kJ•mol-1 |
10.用NA表示阿伏加德罗常数的值.下列叙述中不正确的是( )
| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| B. | 常温常压下,18gH2O中含有的原子总数为3NA | |
| C. | 标准状况下,0.1molCl2溶于水,转移的电子数目小于0.1NA | |
| D. | 常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA |
14.X、Y、Z、M、N是元素周期表中的短周期主族元素.且原子序数依次增大.X原子最外层电子数是内层电子数的2倍,Y、M同主族且M的核电荷数是Y的2倍,Z原子半径在同周期主族元素原子中最大.下列相关说法正确的是( )
| A. | X元素只能形成-种单质 | |
| B. | Y和M元素的最高正价相同 | |
| C. | M、N的最高价氧化物对应水化物的酸性强弱:M>N | |
| D. | Z与Y能形成Z2Y型的离子化合物 |
 .
. .
.