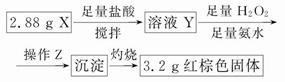
题目内容
Fe2+和I-是两种常见的还原性离子。
(1)向FeSO4溶液中滴加氯水,溶液由浅绿色变成黄色,反应的离子方程式为 ;向KI溶液中滴加氯水,溶液由无色变成黄色,反应的离子方程式: 。
(2)请以FeSO4溶液、KI溶液、氯水为试剂验证I-的还原性强于Fe2+。设计实验方案,补充完成实验步骤、预期现象和结论。其他限选试剂:3 mol·L-1 H2SO4、0.01 mol·L-1 KMnO4、20% KSCN、3%H2O2、淀粉溶液、紫色石蕊溶液。
| 实验步骤 | 预期现象与结论 |
| 步骤1:取2mLFeSO4溶液和2mLKI溶液混合于试管中,再滴加1~2滴氯水。 | ; |
| 步骤2:____________________________________ ____________________________________。 | |
(3)利用(2)提供的试剂证明碘与铁的化合物中铁显+2价,实验操作和现象是:取少量样品溶于水, 。
(1)2Fe2++Cl2=2Fe3++Cl-(3分) 2I-+Cl2=I2+2Cl- (3分)
(2)(6分,各2分)实验步骤
步骤1:…………………………………………预期现象与结论
溶液变成黄色步骤2:向试管中继续滴加几滴20%KSCN溶液
或:向试管中继续滴加几滴淀粉溶液溶液不变血红色,证明I-的还原性强于Fe2+
或:溶液变蓝色,证明I-的还原性强于Fe2+
(3)滴加几滴20%KSCN溶液,无明显现象;再加入过量3%H2O2,溶液变血红色。(4分)
解析试题分析:(1)硫酸亚铁中滴加强化性的氯水,亚铁离子被氧化为铁离子,所以发生溶液变色,所以离子方程式为2Fe2++Cl2=2Fe3++Cl- ;而往碘化钾溶液中同样滴加氯水,还原性的I-被氧化成碘单质,形成棕黄色的碘水溶液,所以离子方程式为2I-+Cl2=I2+2Cl-。
(2)本探究实验的目的是以FeSO4溶液、KI溶液、氯水为试剂验证I-的还原性强于Fe2+ 。要证明I-的还原性强于Fe2+ ,则可以设计让I-和Fe2+ 混合,然后滴加少量的强氧化剂,根据氧化还原规律,还原性强的先被氧化,所以滴加氯水试剂,只要证明先反应生成碘单质,而没有铁离子生成,即可得到结论。所以具体实验情况如下表:实验步骤
步骤1:…………………………………………预期现象与结论
溶液变成黄色步骤2:向试管中继续滴加几滴20%KSCN溶液
或:向试管中继续滴加几滴淀粉溶液溶液不变血红色,证明I-的还原性强于Fe2+
或:溶液变蓝色,证明I-的还原性强于Fe2+
(3)要证明碘与铁的化合物中铁显+2价,实质上就是利用(2)中提供的20%KSCN试剂来检验亚铁离子,所以正确的操作是:取少量样品溶于水,滴加几滴20%KSCN溶液,无明显现象;再加入过量3%H2O2,溶液变血红色,说明碘与铁的化合物中铁显+2价。
考点:本题考查的是氯水的强氧化性、围绕亚铁离子检验的探究性试验。

 快乐5加2金卷系列答案
快乐5加2金卷系列答案硫酸亚铁是重要的亚铁盐,在农业上用作农药,主要治小麦黑穗病,还可以用作除草剂;在工业上用于染色、制造蓝黑墨水和木材防腐等。
(1)新制的绿矾(FeSO4·7H2O)是浅绿色的,但在空气中极易变成黄色或铁锈色的碱式硫酸铁[Fe(OH)SO4],写出该反应的化学方程式: 。
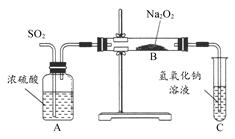
(2)已知FeSO4在不同条件下分解得到产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2;
SO3熔点是16.8℃,沸点是44.8℃。
某研究性学习小组拟用下列装置进行实验探究“在加热条件下FeSO4的分解产物”。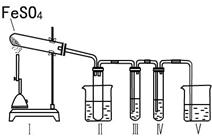
上述装置Ⅲ和Ⅳ用来检验气体产物。试回答下列问题:
①Ⅱ装置烧杯中水的温度应控制在 (选填“0℃、25℃、50℃”),装置Ⅱ的作用是 。
②装置Ⅲ中的试剂可以是 (选填序号,下同),现象是 ,则证明气体产物中含有SO2; 装置Ⅳ中的试剂可以是 。
| A.2 mol/LNa2CO3溶液 |
| B.品红溶液 |
| C.0.5 mol/LBaCl2溶液 |
| D.0.5 mol/LBa(NO3)2 |
F. 淀粉碘化钾溶液
③装置V中试剂为NaOH溶液,发生反应的离子方程式为 。
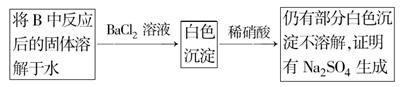
④为了检验固体产物成分,取反应后的固体于试管中,加稀硫酸溶解,将所得溶液分成两份,进行如
下实验:
| 操作步骤 | 预期实验现象 | 预期实验结论 |
| 向其中一份溶液中加入 。 | | 固体中含有Fe2O3 |
| 向另一份溶液中滴加2滴黄色K3[Fe(CN)6]溶液。 | 产生蓝色沉淀 | |
⑤若用22.8 g FeSO4固体做实验,完全分解后,得到11.2 g固体,其中Fe2O3的质量分数=
(精确到0.1%)
FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S。
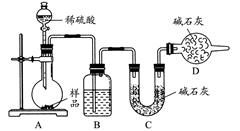
I、经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了制备无水 FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下: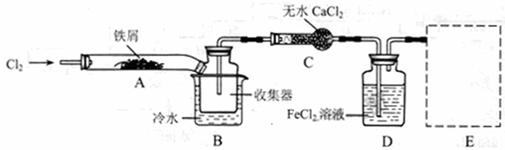
①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④……
⑤体系冷却后,停止通入Cl2,并用干燥的H2赶尽Cl2,将收集器密封。
请回答下列问题:
(1)装置A中反应的化学方程式为 。
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A右端。要使沉积的FeCl3进入收集器,第④步操作是 。
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号) 。
(4)如果没有装置C的设计,会导致 。
(5)用离子方程式表示虚线框E中所增加装置和试剂的作用: 。
(6)用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫,
请写出反应的离子方程式: 。
Ⅱ、反应结束后,将收集器中所得固体完全溶于稀盐酸,小组同学对所得溶液金属阳离子的成分有三种观点:①只有Fe3+;②只有Fe2+;③ 。
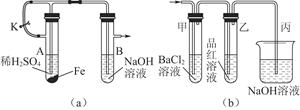
为探究溶液的组成,实验如下:
| 实验步骤 | 实验现象 | 实验结论及反应离子方程式 |
| ①取少量所得溶液于试管中,加入少量KSCN溶液。 | | 说明:假设②不成立,假设①或③成立;的离子方程式是 。 |
| ②另取少量所得溶液于试管中,加入少量酸性 KMnO4溶液。 | 溶液紫红色退去 | 说明: 。 |
综合上述实验分析,所得溶液中含有的金属阳离子有 。