题目内容
“西气东输”工程使东部发达地区的居民告别了管道煤气,用上了天然气。已知某管道煤气的主要成分是H2和CO,其体积比为1∶1;天然气的主要成分是CH4,它们燃烧的热化学方程式为:①2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ/mol ②2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ/mol
③CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.31 kJ/mol
当使用管道煤气的用户改用天然气后,在相同条件下燃烧等体积的可燃气体,理论上所获得的热量,后者大约是前者的多少倍( )
③CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.31 kJ/mol
当使用管道煤气的用户改用天然气后,在相同条件下燃烧等体积的可燃气体,理论上所获得的热量,后者大约是前者的多少倍( )
| A.1.3 | B.3.1 | C.1.6 | D.0.8 |
B
设燃烧2mol甲烷,则等体积的管道煤气中氢气、一氧化碳气体各1mol;
由CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.31 kJ/mol可知,燃烧2mol甲烷放出的热量为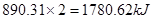 ;燃烧等体积的管道煤气放出的热量为
;燃烧等体积的管道煤气放出的热量为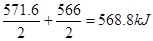 ,理论上所获得的热量甲烷是管道煤气的
,理论上所获得的热量甲烷是管道煤气的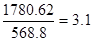 ;
;
由CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.31 kJ/mol可知,燃烧2mol甲烷放出的热量为
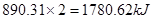 ;燃烧等体积的管道煤气放出的热量为
;燃烧等体积的管道煤气放出的热量为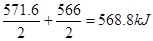 ,理论上所获得的热量甲烷是管道煤气的
,理论上所获得的热量甲烷是管道煤气的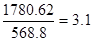 ;
;
练习册系列答案
相关题目

 2NH3(g) ΔH="-92.4" KJ/mol,则N≡N键的键能是 ( )
2NH3(g) ΔH="-92.4" KJ/mol,则N≡N键的键能是 ( ) 2SO3( g ) ;△ H =-QkJ·mol-1在上述条件下分别充入的气体和反应放出的热量 ( Q)如下表所列:根据以上数据,下列叙述正确的是( )
2SO3( g ) ;△ H =-QkJ·mol-1在上述条件下分别充入的气体和反应放出的热量 ( Q)如下表所列:根据以上数据,下列叙述正确的是( )
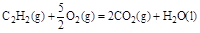 ;△H=-1300kJ/mol的说法中,正确的是( )
;△H=-1300kJ/mol的说法中,正确的是( )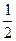 O2(g) = H2O(g) ΔH1=a kJ·mol-1?
O2(g) = H2O(g) ΔH1=a kJ·mol-1? 的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。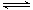 2NH3(g) △H=a kJ·mol-1。试根据表中所列键能数据估算a 的值:_______________。
2NH3(g) △H=a kJ·mol-1。试根据表中所列键能数据估算a 的值:_______________。 __。
__。 则反应
则反应 的
的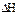 为
为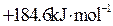


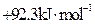
 ,已知断裂1molN-N吸收167kJ热量,生成1mol N≡N放出942kJ热量。根据以上信息和数据,则由N2气体生成1mol气态N4的△H为( )
,已知断裂1molN-N吸收167kJ热量,生成1mol N≡N放出942kJ热量。根据以上信息和数据,则由N2气体生成1mol气态N4的△H为( )