题目内容
4.为探究一溴环己烷( )与NaOH的醇溶液共热发生的是水解反应还是消去反应,甲、乙、丙三位同学分别设计如下三个实验方案:
)与NaOH的醇溶液共热发生的是水解反应还是消去反应,甲、乙、丙三位同学分别设计如下三个实验方案:甲:向反应混合液中滴入稀硝酸中和NaOH,然后再滴入AgNO3溶液,若有淡黄色沉淀生成则可证明发生了消去反应.
乙:向反应混合液中滴入溴水,若溶液颜色很快褪去,则可证明发生了消去反应.[*
丙:向反应混合液中滴入酸性KMnO4溶液,若溶液颜色变浅,则可证明发生了消去反应其中正确的是( )
| A. | 甲 | B. | 乙 | ||
| C. | 丙 | D. | 上述实验方案都不正确 |
分析 甲:消去反应和水解反应都会生成溴离子;
乙:反应后的溶液中有氢氧化钠,溴能够与氢氧化钠反应褪色;
丙:溶液中有溴离子存在,溴离子能够被高锰酸钾溶液氧化.
解答 解:甲:由于无论发生消去反应还是发生水解反应,溶液中都会存在溴离子,无法证明反应类型,故甲错误;
乙:由于反应后的溶液中存在氢氧化钠,氢氧化钠能够与溴能够反应使溴水褪色,所以无法证明反应类型,故乙错误;
丙:由于两种反应的溶液中都有溴离子存在,溴离子能够被高锰酸钾溶液氧化,所以无法判断反应类型,故丙错误;
故选D.
点评 本题考查化学实验方案的评价,涉及卤代烃的水解反应和消去反应的验证,注意涉及实验方案的严密性,本题难度中等.

练习册系列答案
相关题目
14.下列溶液中能大量共存的微粒的是( )
| A. | 水电离出的C(H+)=10-13mol/L的溶液中K+、NO3-、Br-、Cl- | |
| B. | 含有大量NO3-的水溶液:I-、Fe3+、H+、Na+ | |
| C. | 弱碱性溶液中HCO3-、NH4+、C2H5O-、MnO4- | |
| D. | 无色透明溶液中:Ba2+、S2-、Cu2+、AlO2- |
12.氢氧燃料电池是一种新能源.图为氢氧燃料电池示意图.下列说法不正确的是( )
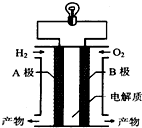

| A. | 电子由B极通过导线流向A极 | |
| B. | A极是负极,B极是正极 | |
| C. | 该装置能将化学能转化为电能 | |
| D. | 产物为无污染的水,属于环境友好电池 |
19.氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的( )
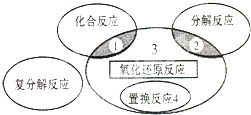

| A. | 4Fe(0H)2+O2+2H2O═4Fe(OH)3 | B. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2 O+CO2↑ | ||
| C. | 4NH3+5O2 $\frac{\underline{催化剂}}{△}$4NO+6H2O | D. | Zn+H2SO4═ZnSO4+H2↑ |
9.某温度下气体反应达到化学平衡,平衡常数K=$\frac{c(A)•c2(B)}{c2(E)•c(F)}$,恒容时,若温度适当降低,F的浓度增加.下列说法中正确的是( )
| A. | 增大c(A)、c(B),K增大 | |
| B. | 降低温度,正反应速率增大 | |
| C. | 该反应的焓变为负值 | |
| D. | 该反应的化学方程式为2E(g)+F(g)?A(g)+2B(g) |
16.下列物质属于同分异构体的是( )
| A. | 葡萄糖与蔗糖 | B. | 蔗糖与麦芽糖 | C. | 动物油和脂肪 | D. | 淀粉和纤维素 |
14.设NA 为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 1mol羟基中电子数为10NA | |
| B. | 常温下,1L 0.1mol/L的NH4NO3的溶液中氮原子数为0.2NA | |
| C. | 在反应KIO3+6HI=KI+3 I2+3 H2O中,每生成3mol I2转移的电子数为6NA | |
| D. | 常温常压下,22.4L乙烯中C-H键数为4NA |
 如图是一种形状酷似一条小狗的有机物.化学家Tim Rickard将其取名为“doggycene”.doggycene的分子式为C26H26.该分子中所有碳原子可能(填“可能”或“不可能”)处予同一平面.
如图是一种形状酷似一条小狗的有机物.化学家Tim Rickard将其取名为“doggycene”.doggycene的分子式为C26H26.该分子中所有碳原子可能(填“可能”或“不可能”)处予同一平面.