题目内容
已知CH4(g)+2O2(g)→CO2(g)+2H2O(g)△H═-Q1;2H2(g)+O2(g)→2H2O(g)△H═-Q2;H2O(g)→H2O(l)△H═-Q3常温下,取体积比为4:1的甲烷和H2的混合气体112L(标准状况下)经完全燃烧后恢复到常温,则放出的热量为( )
A.4Q1+0.5Q2
B.4Q1+Q2+10Q3
C.4Q1+2Q2
D.4Q1+0.5Q2+9Q3
【答案】分析:根据盖斯定律书写生成甲烷、氢气生成液体水的热化学反应方程式,根据n=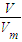 计算混合气体的物质的量,结合体积分数计算甲烷、氢气各自物质的量,结合热化学方程式计算放出的热量.
计算混合气体的物质的量,结合体积分数计算甲烷、氢气各自物质的量,结合热化学方程式计算放出的热量.
解答:解:已知:①、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H═-Q1;
②、2H2(g)+O2(g)=2H2O(g)△H═-Q2;
③、H2O(g)=H2O(l)△H═-Q3;
根据盖斯定律,①+2×③得CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H═-Q1-2Q3,
根据盖斯定律,②+2×③的2H2(g)+O2(g)=2H2O(l)△H═-Q2-2Q3,
112L体积比为4:1的甲烷和H2的混合气体的物质的量为 =5mol,
=5mol,
故甲烷的物质的量我5mol× =4mol,完全燃烧生成液体水放出的热量为(Q1+2Q3)×
=4mol,完全燃烧生成液体水放出的热量为(Q1+2Q3)× =4(Q1+2Q3),
=4(Q1+2Q3),
氢气的物质的量为5mol-4mol=1mol,完全燃烧生成液体水放出的热量为(Q2+2Q3)×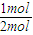 =0.5(Q2+2Q3),
=0.5(Q2+2Q3),
故甲烷、氢气完全燃烧,放出的热量为:4(Q1+2Q3)+0.5(Q2+2Q3)=4Q1+0.5Q2+9Q3,
故选D.
点评:考查反应热的有关计算,难度中等,注意常温下生成的水是液态,利用盖斯定律书物质燃烧生成液态水的热化学方程式是解题关键.
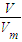 计算混合气体的物质的量,结合体积分数计算甲烷、氢气各自物质的量,结合热化学方程式计算放出的热量.
计算混合气体的物质的量,结合体积分数计算甲烷、氢气各自物质的量,结合热化学方程式计算放出的热量.解答:解:已知:①、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H═-Q1;
②、2H2(g)+O2(g)=2H2O(g)△H═-Q2;
③、H2O(g)=H2O(l)△H═-Q3;
根据盖斯定律,①+2×③得CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H═-Q1-2Q3,
根据盖斯定律,②+2×③的2H2(g)+O2(g)=2H2O(l)△H═-Q2-2Q3,
112L体积比为4:1的甲烷和H2的混合气体的物质的量为
 =5mol,
=5mol,故甲烷的物质的量我5mol×
 =4mol,完全燃烧生成液体水放出的热量为(Q1+2Q3)×
=4mol,完全燃烧生成液体水放出的热量为(Q1+2Q3)× =4(Q1+2Q3),
=4(Q1+2Q3),氢气的物质的量为5mol-4mol=1mol,完全燃烧生成液体水放出的热量为(Q2+2Q3)×
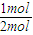 =0.5(Q2+2Q3),
=0.5(Q2+2Q3),故甲烷、氢气完全燃烧,放出的热量为:4(Q1+2Q3)+0.5(Q2+2Q3)=4Q1+0.5Q2+9Q3,
故选D.
点评:考查反应热的有关计算,难度中等,注意常温下生成的水是液态,利用盖斯定律书物质燃烧生成液态水的热化学方程式是解题关键.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
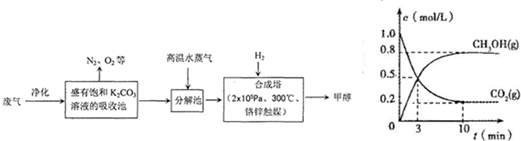
 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据: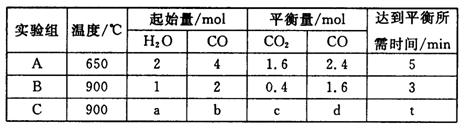
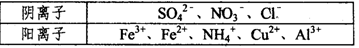
 CO2(g)+2H2O(l) △H1=a kJ/mol欲计算反应CH4(g)+4NO(g)
CO2(g)+2H2O(l) △H1=a kJ/mol欲计算反应CH4(g)+4NO(g)