题目内容
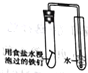
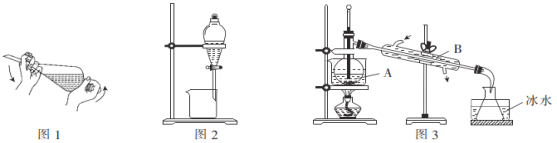
【题目】下列实验装置正确且能达到实验目的的是
A | B | C | D | |
实验目的 | 比较盐酸、碳酸、硅酸的酸性强弱 | 检验碳与浓H2SO4反应的产物中含CO2 | 验证铁的析氢腐蚀 | 模拟电解精炼铜 |
实验装置 |
|
|
|
|
A. A B. B C. C D. D
【答案】D
【解析】A.盐酸易挥发,盐酸与硅酸钠也能反应生成硅酸,则不能比较碳酸、硅酸的酸性强弱,故A错误;B. 碳与浓H2SO4反应的产物中含CO2,也含有二氧化硫,二氧化硫也能使澄清的石灰水变浑浊,检验二氧化碳之前需要除去二氧化硫,品红溶液不能完全除去二氧化硫,故B错误;C.食盐水为中性,发生吸氧腐蚀,酸性电解质才可发生析氢腐蚀,故C错误;D.电解精炼铜,粗铜为阳极,纯铜为阴极,电解质为铜盐溶液,根据图示电流方向,粗铜为阳极,纯铜为阴极,电解质为铜盐溶液,故D正确;故选D。

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目