题目内容
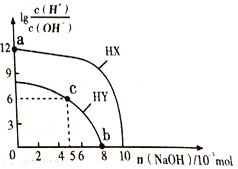
【题目】常温下,向浓度均为0.1 molL-1、体积均为100mL的两种一元酸HX、HY的溶液中,分别加入NaOH 固体,lg![]() 随加入NaOH的物质的量的变化如图所示(忽略加入NaOH固体导致溶液温度的变化)。下列叙述正确的是.
随加入NaOH的物质的量的变化如图所示(忽略加入NaOH固体导致溶液温度的变化)。下列叙述正确的是.
A. HX的酸性弱于HY
B. c点溶液中c(Y-)<c(HY)
C. a点由水电离出的c(H+)=10-12 molL-1
D. b点溶液中离子浓度大小关系为c(Y-)+c(HY)=c(Na+)+0.02 molL-1
【答案】D
【解析】A.lg![]() 越大,溶液中氢离子浓度越大,未加NaOH时,HX溶液中lg
越大,溶液中氢离子浓度越大,未加NaOH时,HX溶液中lg![]() 的值大,所以HX的酸性大于HY,故A错误;B.c点lg
的值大,所以HX的酸性大于HY,故A错误;B.c点lg![]() =6,则溶液中c(H+)=10-4mol/L,此时消耗的NaOH为0.005mol,则溶液中的溶质为NaY和HY,由于溶液显酸性,所以HY的电离程度大于NaY的水解程度,所以c(Y-)>c(HY),故B错误;C.a点lg
=6,则溶液中c(H+)=10-4mol/L,此时消耗的NaOH为0.005mol,则溶液中的溶质为NaY和HY,由于溶液显酸性,所以HY的电离程度大于NaY的水解程度,所以c(Y-)>c(HY),故B错误;C.a点lg![]() =12,则溶液中c(H+)=0.1mol/L,溶液中水电离的c(H+)=
=12,则溶液中c(H+)=0.1mol/L,溶液中水电离的c(H+)=![]() =10-13molL-1,故C错误; D.b点lg
=10-13molL-1,故C错误; D.b点lg![]() =0,则溶液中c(H+)= c(OH-)=10-7mol/L,此时消耗的NaOH为0.008mol,c(Na+)=0.08 mol/L,根据物料守恒,c(Y-)+c(HY)=0.1 mol/L,因此c(Y-)+c(HY)=c(Na+)+0.02 molL-1,故D正确;故选D。
=0,则溶液中c(H+)= c(OH-)=10-7mol/L,此时消耗的NaOH为0.008mol,c(Na+)=0.08 mol/L,根据物料守恒,c(Y-)+c(HY)=0.1 mol/L,因此c(Y-)+c(HY)=c(Na+)+0.02 molL-1,故D正确;故选D。

练习册系列答案
相关题目
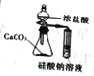
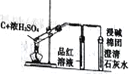
【题目】下列实验装置正确且能达到实验目的的是
A | B | C | D | |
实验目的 | 比较盐酸、碳酸、硅酸的酸性强弱 | 检验碳与浓H2SO4反应的产物中含CO2 | 验证铁的析氢腐蚀 | 模拟电解精炼铜 |
实验装置 |
|
|
|
|
A. A B. B C. C D. D