题目内容
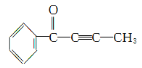
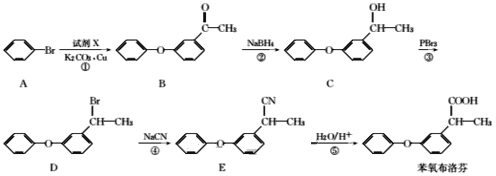
【题目】化合物A是基本有机化工原料,由A合成高分子化合物C和![]() 的合成路线如图(部分反应条件略去):
的合成路线如图(部分反应条件略去):

已知:①R-Cl![]() R-CN
R-CN
②R-CN![]() R-COOH
R-COOH
③![]()
回答下列问题:
(1)A的化学名称是__。
(2)C分子中所含官能团的名称是__;G→H的反应类型是__。
(3)F→G的化学方程式是__。
(4)B的同分异构体中,某种同分异构体M与H2加成的是产物(C5H10O2),其中含有酯基并且核磁共振氢谱有4组峰,且峰面积比为6∶2∶1∶1,则M的结构简式可能是__、___。
【答案】丙烯 酯基 取代反应 CH2=CHCH2OH+![]()
![]()
![]()
![]()
![]()
【解析】
A为C3H6,A发生加成反应生成的B为CH3CH=CHCOOCH3,则A结构简式为CH2=CHCH3,B发生加聚反应生成的C为聚丁烯酸甲酯,其结构简式为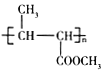 ,聚丁烯酸甲酯发生碱性水解反应然后酸化得到聚合物D,D的结构简式为
,聚丁烯酸甲酯发生碱性水解反应然后酸化得到聚合物D,D的结构简式为 ;A与Cl2在光照条件下发生反应生成E,D发生水解反应生成F,F和C4H5Cl发生信息②的加成反应生成G,则F分子结构中含有一个碳碳双键,C4H5Cl分子结构中含有两个碳碳双键,结合F分子式C3H6O可知,F结构简式为CH2=CHCH2OH、E结构简式为CH2=CHCH2Cl,X为2-氯-1,3-丁二烯(
;A与Cl2在光照条件下发生反应生成E,D发生水解反应生成F,F和C4H5Cl发生信息②的加成反应生成G,则F分子结构中含有一个碳碳双键,C4H5Cl分子结构中含有两个碳碳双键,结合F分子式C3H6O可知,F结构简式为CH2=CHCH2OH、E结构简式为CH2=CHCH2Cl,X为2-氯-1,3-丁二烯(![]() ),F和X发生加成反应生成G,G与NaCN发生取代反应生成H,H在酸性条件下水解生成
),F和X发生加成反应生成G,G与NaCN发生取代反应生成H,H在酸性条件下水解生成 ,由此推出H为
,由此推出H为![]() ,G为
,G为![]() ,由此分析解题。
,由此分析解题。
(1)A的结构简式为CH2=CHCH3,其化学名称是丙烯;
(2)C的结构简式为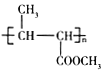 ,分子中含有的官能团的名称是酯基;G为
,分子中含有的官能团的名称是酯基;G为![]() ,与NaCN发生取代反应生成
,与NaCN发生取代反应生成![]() ;反应类型为取代反应;
;反应类型为取代反应;
(3)F为CH2=CHCH2OH,其和2-氯-1,3-丁二烯(![]() )发生加成反应生成
)发生加成反应生成![]() 的化学方程式是CH2=CHCH2OH+
的化学方程式是CH2=CHCH2OH+![]()
![]()
![]() ;
;
(4)B为CH3CH=CHCOOCH3,其分子式为C5H8O2,分子结构中含有酯基,则它的同分异构体中,与B具有相同的官能团且能发生银镜反应,说明含有HCOO-,烃其分子式为C4H7O—,其中结构C=C-C-C中连接HCOO-有4种、C-C=C-C中连接HCOO-有2种,C=C(C)2中连接HCOO-有2种,即满足条件的B的同分异构体共有8种;其中![]() 和
和![]() 与H2加成的产物(C5H10O2)的核磁共振氢谱有4组峰,且峰面积比为6∶2∶1∶1。
与H2加成的产物(C5H10O2)的核磁共振氢谱有4组峰,且峰面积比为6∶2∶1∶1。

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案【题目】苯甲酸是一种重要的化工原料。实验室合成苯甲酸的原理及装置示意图(加热、 夹持及辅助仪器省略)和一些相关信息如下:

名称 | 性状 | 熔点(℃) | 沸点(℃) | 密度(g/mL) | 溶解性 | |
水 | 乙醇 | |||||
甲苯 | 无色液体易燃易挥发 | ﹣95 | 110.6 | 0.8669 | 不溶 | 互溶 |
苯甲酸 | 白色片状或针状晶体 | 112.4(100℃左右升华) | 248 | 1.2659 | 微溶 | 易溶 |
苯甲酸在水中的溶解度如表:
温度/℃ | 4 | 18 | 75 |
溶解度/g | 0.2 | 0.3 | 2.2 |
某学习小组在实验室制备、分离、提纯苯甲酸,并测定所得样品的纯度,步骤如下:
Ⅰ.在b 中加入 2.7 mL 甲苯、100 mL水和几片碎瓷片,开动电动搅拌器,a中通水。将b 中的液体加热至沸腾,分批加入 8.5 g 高锰酸钾,继续搅拌约5 h,停止加热和搅拌,静置。
Ⅱ.在反应混合物中加入一定量草酸(H2C2O4)充分反应,过滤、洗涤,将滤液放在冰水浴中冷却,再用浓盐酸酸化,苯甲酸全部析出后减压过滤,冷水洗涤,干燥,得到粗产品。
Ⅲ.称取m g产品,配成 100 mL乙醇溶液,移取25.00 mL溶液于锥形瓶,滴加2~3滴酚酞,然后用标准浓度KOH溶液滴定。请回答下列问题:
(1)装置a的作用___________
(2)分离提纯过程中加入的草酸是一种二元弱酸,反应过程中有酸式盐和无色气体生成。加入草酸的作用_______,请用离子方式表示该反应原理_____。
(3)产品减压过滤时用冷水洗涤的原因是_____________
(4)选用下列________(选填字母)操作,可以将粗产品进一步提纯。
A 溶于水后过滤 B 溶于乙醇后蒸馏
C 用甲苯萃取后分液 D 升华
(5)测定纯度步骤中,滴定终点溶液的颜色变化是__。若m=1.200 g,滴定时用去0.1200 mol·L-1 标准KOH溶液20.00 mL,则所得产品中苯甲酸的质量分数为______。
【题目】某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:

沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀的pH | 2.3 | 7.6 | 4.4 |
完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(1)酸浸后加入H2O2的目的是________________,调pH的最适宜范围为________________。
(2)调pH过程中加入的试剂最好是___________。
A. NaOH B. CuO C.NH3·H2O D.HCl
(3)煮沸CuSO4溶液的原因是_________。向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式_________。
(4)过滤后的沉淀表面通常附着有一些杂质离子,为得到纯净产物,需要进行洗涤,确定沉淀洗涤干净的操作及现象是_________。
(5)称取所制备的CuCl样品0.2500g置于一定量的0.5mol·L-1FeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000 mol·L-1的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液25.00mL。有关的化学反应为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+。计算该CuCl样品的质量分数__________。