题目内容
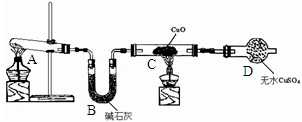
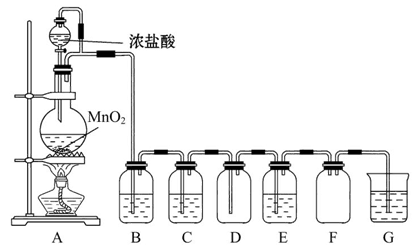
工业尾气中氮氧化物通常采用氨催化吸收法,其原理是NH3与NOx在催化剂作用下反应生成无毒的物质。某校活动小组同学采用以下装置和步骤模拟工业上氮氧化物的处理过程。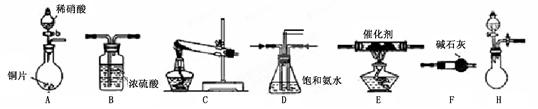
I.探究制取NH3的方法
(1)在上述装置中,H能快速、简便制取NH3,装置中需要添加的反应试剂为 。
(2)为探究更好的实验效果,活动小组同学采用上述C装置来制取氨气,在控制实验条件相同的情况下,获得下表中实验数据。
| 试剂组合序号 | 固体试剂 | NH3体积(mL) | |
| a | 6.0 g Ca(OH)2(过量) | 5.4 g NH4Cl | 1344 |
| b | 5.4g (NH4)2SO4 | 1364 | |
| c | 6.0 g NaOH(过量) | 5.4 g NH4Cl | 1568 |
| d | 5.4g (NH4)2SO4 | 1559 | |
| e | 6.0 g CaO(过量) | 5.4 g NH4Cl | 1753 |
| f | 5.4 g (NH4)2SO4 | 1792 | |
分析表中数据,你认为哪种方案制取氨气的效果最好 (填序号),从该方案选择的原料分析制气效果好的可能原因是 。
II.模拟尾气处理
活动小组同学选用上述部分装置,按下列顺序连接成模拟尾气处理装置进行实验。
(1)请从上述装置中选择你认为合理的进行补充(所选装置不能重复)。
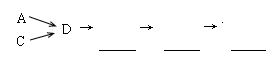
(2)A中反应的离子方程式为 。
(3)D装置的作用有:使气体混合均匀、调节气流速度、 。
(4)D装置中的液体还可换成 (填序号)。
a.H2O b.CCl4 c.浓H2SO4 d.CuSO4溶液
(5)该小组同学所设计的模拟尾气处理装置中还存在一处明显的缺陷是 。
I.(1)生石灰与浓氨水(或烧碱与浓氨水) (答化学式给分)(2分)
(2)f (2分) (NH4)2SO4受热不分解,CaO又有吸水作用(合理答案均给分)(2分)
II.(1)F E B (2分)
(2)3Cu + 2NO3-+8H+ 3Cu2+ + 2NO↑ +4H2O (2分)
3Cu2+ + 2NO↑ +4H2O (2分)
(3)防止氨气溶解(或防止倒吸)(2分)
(4)b(2分)
(5)未反应的NO无法处理,会污染环境 (2分)
解析试题分析:(1)依据装置分析制备氨气气体是利用液体通过分液漏斗滴入烧瓶中不加热进行的反应,实验目的是制取、干燥和收集氨气的装置,制备氨气先干燥再收集,氨气比空气轻,应用向下排气法收集;制备氨气可以利用浓氨水滴入氧化钙或固体氢氧化钠或碱石灰,溶解放热时一水合氨分解生成氨气;
(2)因为NH4Cl受热易分解,生成的部分NH3和HCl又重新结合成NH4Cl,而用NaOH或Ca(OH)2作反应物产生的水较多,吸收的NH3较多,由表中数据可以看出,f制NH3产率最高;
II.(1)混合气体干燥后进入反应装置,然后用浓硫酸吸收没有反应的氨气。
(2)稀硝酸具有强氧化性,与铜发生氧化还原反应生成硝酸铜和NO等,反应的离子方程式为3Cu + 2NO3-+8H+ 3Cu2+ + 2NO↑ +4H2O;
3Cu2+ + 2NO↑ +4H2O;
(3)D装置使气体混合均匀、调节气流速度,另外,氨气难溶于饱和氨水,可防止倒吸;
(4)氨气可溶于硫酸铜溶液、水以及硫酸中,可产生倒吸,氨气为极性分子,不溶于非极性溶剂,可用CCl4代替饱和氨水;
(5)缺少尾气处理装置,过量的NO会污染空气。
考点:考查氮的氧化物的性质以及对环境的影响。

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案清洗和制绒是硅晶片制作的重要步骤之一,硅片化学清洗的主要目的是除去硅片表面杂质(如某些有机物,无机盐,金属、Si、SiO2粉尘等)。常用的化学清洗剂有高纯水、有机溶剂、双氧水、浓酸、强碱等。其中去除硅的氧化物,通常用一定浓度的HF溶液,室温条件下将硅片浸泡1至数分钟。制绒是在硅片表面形成金字塔形的绒面,增加硅对太阳光的吸收。单晶制绒通常用NaOH、Na2SiO3等混合溶液在75~90℃反应25~35 min,效果良好。回答下列问题
Ⅰ.(1)写出晶片制绒反应的离子方程式 ,对单晶制绒1990年化学家Seidel提出了一种的电化学模型,他指出Si与NaOH溶液的反应,首先是Si与OH一反应,生成SiO44一,然后SiO44一迅速水解生成H4SiO4。基于此原理分析反应中氧化剂为 。
(2)本校化学兴趣小组同学,为验证Seidel的理论是否正确,完成以下实验:
| | 实验事实 |
| 事实一 | 水蒸汽在600℃时可使粉末状硅缓慢氧化并放出氢气。 |
| 事实二 | 盛放于铂或石英器皿中的纯水长时间对粉末状还原硅无腐蚀作用。 |
| 事实三 | 普通玻璃器皿中的水仅因含有从玻璃中溶出的微量的碱便可使粉末状硅在其中缓慢溶解。 |
| 事实四 | 在野外环境里,用较高百分比的硅铁粉与干燥的Ca(OH)2和NaOH,点着后焖烧,可剧烈放出H2。 |
| 事实五 | 1g(0.036mo1)Si和20mL含有lgNaOH(0.025mol)的溶液,小心加热(稍微预热),收集到约1700mL H2,很接近理论值(1600mL)。 |
Ⅱ.在工业中利用镁制取硅:2Mg+SiO2
 2MgO+Si,同时有副反应发生:2Mg+Si
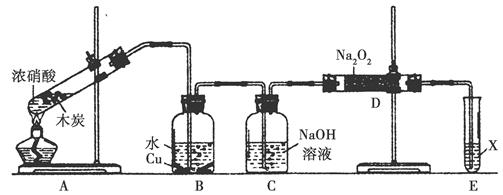
2MgO+Si,同时有副反应发生:2Mg+Si Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4(硅烷),SiH4在常温下是一种不稳定、易分解的气体。如图是进行Mg与SiO2反应的实验装置:
Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4(硅烷),SiH4在常温下是一种不稳定、易分解的气体。如图是进行Mg与SiO2反应的实验装置:
由于氧气的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。 a.石灰石 b.锌粒 c.纯碱
(4)实验开始时,必须先通入X气体,再加热反应物,其理由是______________________________,当反应开始后,移走酒精灯反应能继续进行,其原因是___________________________。
(5)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸。可观察到闪亮的火星,产生此现象的原因用化学方程式表示为_______________________________________。


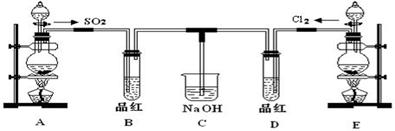
 MnCl2+Cl2↑+2H2O。若有6 mol的HCl参加反应,则转移的电子总数为 。
MnCl2+Cl2↑+2H2O。若有6 mol的HCl参加反应,则转移的电子总数为 。