题目内容
【题目】两种金属混合物粉末15g,与足量的盐酸反应生成标准状况下11.2L氢气,符合上述情况的金属混合物是( )
A.Mg、FeB.Zn、AgC. Fe、ZnD.Mg、Al
【答案】A
【解析】
11.2L氢气的物质的量为:n=![]() =0.5mol,假设金属都为+2价,则金属混合物的平均摩尔质量为:
=0.5mol,假设金属都为+2价,则金属混合物的平均摩尔质量为:![]() =30g/mol;
=30g/mol;
A.Mg的相对原子质量为24,Fe的相对原子质量为56,平均摩尔质量可能等于30g/mol,符合题意,选项A正确;
B.Zn的相对分子质量为65,Ag与盐酸不反应,生成0.5mol氢气所以Zn的质量为0.5mol×65g/mol=32.5g,大于15g,不符合题意,选项B错误;
C.Fe的相对原子质量为56,Zn的相对分子质量为65,平均摩尔质量大于30g/mol,不符合题意,选项C错误;
D.Mg的相对原子质量为24,当Al的化合价为+2价时,可看成其相对原子质量为:27×2/3=18g/mol,镁和铝的摩尔质量都小于30g/mol,不符合题意,选项D错误;
答案选A。

【题目】根据杂化轨道理论和价电子对互斥理论模型判断,下列分子或离子的中心原子杂化方式及空间构型正确的是( )
选项 | 分子或离子 | 中心原子杂化方式 | 价电子对互斥理论模型 | 分子或离子的空间构型 |
A | H2O | sp | 直线形 | 直线形 |
B | BBr3 | sp2 | 平面三角形 | 三角锥形 |
C | PCl3 | sp2 | 四面体形 | 平面三角形 |
D | CO32- | sp2 | 平面三角形 | 平面三角形 |
A.AB.BC.CD.D
【题目】某强酸性无色溶液中可能含下表离子中的若干种离子。
阳离子 | Mg2+、NH4+、Ba2+、Al3+、Fe2+ |
阴离子 | SiO32-、MnO4-、Cl-、NO3-、SO42- |
实验Ⅰ:取少量该强酸性溶液A进行如下实验。
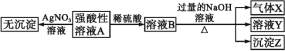
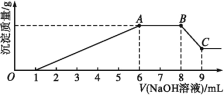
实验Ⅱ:为了进一步确定该溶液的组成,取100 mL原溶液A,向该溶液中滴加1 mol·L-1的NaOH溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图所示。
回答下列问题:
(1)不进行实验就可以推断出,上表中的离子一定不存在的有________种。
(2)通过实验Ⅰ可以确定该溶液中一定存在的阴离子是_________。检验气体X的方法是_______________;沉淀Z的化学式为_____________。
(3)写出实验Ⅱ的图示中BC段对应反应的离子方程式:________________。
(4)A点对应的固体质量为____ g。
(5)通过上述信息,推算该溶液中阴离子的浓度为________ mol·L-1。