题目内容
【题目】下列除去杂质的方法中正确的是( )
A.乙烷中混有乙烯,加入氢气在一定条件下充分反应
B.乙醇中混有乙酸,加入NaOH溶液后,用分液漏斗分液
C.除去乙烯中杂质气体:将实验室制得的乙烯气体通入NaOH 溶液
D.溴苯中混有溴,加入KI溶液后,用分液漏斗分液
【答案】C
【解析】解:A.乙烷中混有乙烯,加入氢气在一定条件下充分反应,会使乙烷中混有氢气,故A错误;
B.乙醇中混有乙酸,加入NaOH溶液后,溶液不分层,不能利用分液漏斗分离,故B错误;
C.乙烯与氢氧化钠不反应,故C正确;
D.溴苯中混有溴,加入KI溶液后,溴与KI反应生成碘,使溴苯中混有碘,故D错误.
故选C.

【题目】下列离子组在给定条件下离子共存判断及反应的离子方程式均正确的是( )
选项 | 条件 | 离子组 | 离子共存判断及反应的离子方程式 |
A | 滴加氨水 | Na+、Al3﹣、Cl﹣、NO | 不能大量共存, |
B | 由水电离出的H+浓度为1×10﹣12molL﹣1 | NH4+、Na+、NO | 一定能大量共存,NH4++H2ONH3H2O+H+ |
C | pH=1的溶液 | Fe2+、Al3+、SO | 不能大量共存,5Fe2++MnO4﹣+8H+═Mn2++5Fe3++4H2O |
D | 通入少量SO2气体 | K+、Na+、ClO﹣、SO | 不能大量共存,2ClO﹣+SO2+H2O═2HClO+SO |
A.A
B.B
C.C
D.D
【题目】(一)为了达到下表中的实验要求,请选择合适的试剂及方法,将其标号填入对应的空格中。
实验要求 | 试剂及方法 | ||
鉴别Na2SO4溶液和NaCl溶液 | A.分别加入氯化钡溶液,观察现象 | ||
证明盐酸溶液呈酸性 | B.将气体分别通过盛有品红溶液的洗气瓶 | ||
鉴别二氧化硫和二氧化碳 | C.加入几滴碘水,观察现象 | ||
检验淘米水中是否含有淀粉 | D.在溶液滴加紫色石蕊,溶液变红 | ||
(二).甲、乙两同学用下图所示装置进行实验,探究硝酸与铁反应的产物 .
文献记载:I.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,其生成的产物有+4、+2、-3价等氮的化合物.
II.FeSO4+NOFe(NO)SO4(棕色)△H<0.
III.NO2和NO都能被KMnO4氧化吸收.
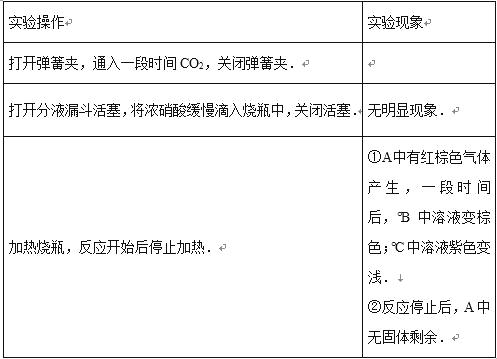
甲的实验操作和现象记录如下:
|
请回答下列问题:
(1)滴入浓硝酸加热前没有明显现象的原因是 .
(2)检验是否生成-3价氮的化合物,应进行的实验操作是 .
(3)证明A溶液中是否含有Fe3+ , 选择的药品是(填序号)( )
A.铁粉
B.溴水
C.铁氰化钾溶液
D.硫氰化钾溶液.
(4)根据实验现象写出A中一定发生反应的化学方程式