题目内容
4.化合物G是一种重要的医药中间体,其中一种合成路线如下: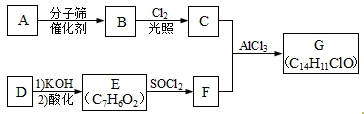
已知下列信息:
①直链烷烃A的相对分子质量为100
②B不能与溴水反应而使之褪色,能使酸性KMnO4溶液褪色,核磁共振氢谱显示有4种氢
③HCHO$→_{(2)酸化}^{(1)KOH}$HCOOH+CH3OH
④2RCOOH+SOCl2→2RCOCl+H2O+SO2↑
⑤
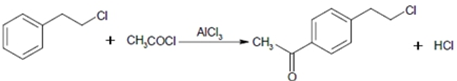
回答下列问题:
(1)G的结构简式为
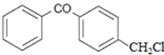 .
.(2)以B为原料经以下步骤可合成一种医用麻醉药品苯佐卡因:
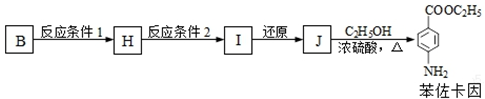
反应条件1所选用的试剂为浓硝酸、浓硫酸,反应条件2所选用的试剂为酸性高锰酸钾溶液,I的结构简式为
 .
.
分析 (1)设直链烷烃A的分子式为CnH2n+2,相对分子质量为100,则14n+2=100,解得n=7,故A的分子式为C7H16,在催化剂条件下得到B,B与氯气发生取代反应生成C为氯代烃,C与F发生信息⑤中的取代反应生成G,结合分子式中碳原子数目,可知B、C分子中碳原子数目为7,B不能与溴水反应而使之褪色,能使酸性KMnO4溶液褪色,说明A发生结构重整得到B为芳香烃,则B为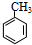 ,C为
,C为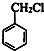 .D发生信息③中的反应得到E,E发生信息④中的反应得到F,则E中含有-COOH,E的不饱和度为$\frac{7×2+2-6}{2}$=5,应还含有苯环,可推知E为
.D发生信息③中的反应得到E,E发生信息④中的反应得到F,则E中含有-COOH,E的不饱和度为$\frac{7×2+2-6}{2}$=5,应还含有苯环,可推知E为 ,D为
,D为 ,则F为
,则F为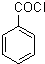 ,由信息⑤可知
,由信息⑤可知 中-CH2Cl对位H原子被
中-CH2Cl对位H原子被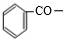 取代生成G,故G的结构简式为:
取代生成G,故G的结构简式为: .
.
(2)J和乙醇发生酯化反应生成苯佐卡因,则J为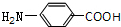 ,I为
,I为 ,甲苯与浓硝酸、浓硫酸在加热条件下发生硝化反应生成H为
,甲苯与浓硝酸、浓硫酸在加热条件下发生硝化反应生成H为 ,H为酸性高锰酸钾溶液氧化生成
,H为酸性高锰酸钾溶液氧化生成 .
.
解答 解:(1)设直链烷烃A的分子式为CnH2n+2,相对分子质量为100,则14n+2=100,解得n=7,故A的分子式为C7H16,在催化剂条件下得到B,B与氯气发生取代反应生成C为氯代烃,C与F发生信息⑤中的取代反应生成G,结合分子式中碳原子数目,可知B、C分子中碳原子数目为7,B不能与溴水反应而使之褪色,能使酸性KMnO4溶液褪色,说明A发生结构重整得到B为芳香烃,则B为 ,C为
,C为 .D发生信息③中的反应得到E,E发生信息④中的反应得到F,则E中含有-COOH,E的不饱和度为$\frac{7×2+2-6}{2}$=5,应还含有苯环,可推知E为
.D发生信息③中的反应得到E,E发生信息④中的反应得到F,则E中含有-COOH,E的不饱和度为$\frac{7×2+2-6}{2}$=5,应还含有苯环,可推知E为 ,D为
,D为 ,则F为
,则F为 ,由信息⑤可知
,由信息⑤可知 中-CH2Cl对位H原子被
中-CH2Cl对位H原子被 取代生成G,故G的结构简式为:
取代生成G,故G的结构简式为: ,故答案为:
,故答案为: ;
;
(2)J和乙醇发生酯化反应生成苯佐卡因,则J为 ,I为
,I为 ,甲苯与浓硝酸、浓硫酸在加热条件下发生硝化反应生成H为
,甲苯与浓硝酸、浓硫酸在加热条件下发生硝化反应生成H为 ,H为酸性高锰酸钾溶液氧化生成
,H为酸性高锰酸钾溶液氧化生成 ,
,
故答案为:浓硝酸、浓硫酸;酸性高锰酸钾溶液; .
.
点评 本题考查有机物的推断,注意根据给予的信息及有机物分子式进行推断,较好的考查学生自学能力、分析推理能力、知识迁移运用,是对有机化学基础的综合考查,难度中等.

| A. | 常温常压下,11.2LN2和NO的混合气体所含的原子数为NA | |
| B. | 1mol C8H18分子中,共价键总数为25NA | |
| C. | 标准状况下,22.4L盐酸含有nA个HCl分子 | |
| D. | 含0.1molH2O2的水溶液跟MnO2充分作用,反应过程中转移的电子总数为0.2NA |
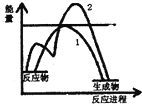 对于CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O反应有关叙述正确的是( )
对于CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O反应有关叙述正确的是( )| A. | 浓硫酸在该反应中起着降低反应活化能和提高原料转化率作用 | |
| B. | 该反应属于消去反应 | |
| C. | 如图表示放热反应的图象.曲线1表示未加催化剂, 则曲线2表示加了催化剂 | |
| D. | 该反应为放热反应,故升髙温度正反应速度减小,逆反应速度加快 |
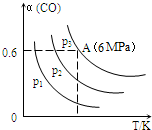
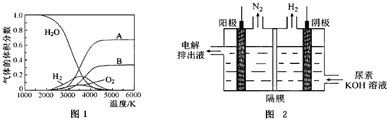
| A. | p1>p2>p3 | |
| B. | 若断裂碳氢键、氢氢键的速率相等,则该反应为平衡状态 | |
| C. | 已知从反应开始到平衡点A需要时间10min.在0~10分钟内的平均速率v(H2)=0.18mol/(L•min) | |
| D. | A点的平衡常数Kp=$\frac{1}{64}$(Kp是用平衡时各组分的分压代替其浓度的平衡常数.组分分压=混合气体总压强X该组分的物质的量分数) |
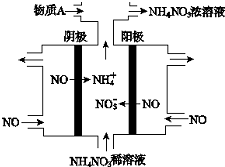
| A. | 阳极上的电极反应为:NO•3e-+4OH-=NO3-+2H2O | |
| B. | 电解生成1 mol NH4NO3 时,转移5NA电子 | |
| C. | 电解质溶液中,NO3-离子向阴极移动 | |
| D. | 为了使电解产物全部转化为NH4NO3,需补充的物质A为稀硝酸 |
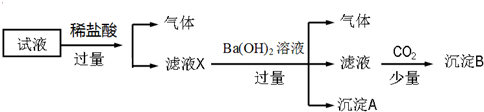
下列说法正确的是( )
| A. | 无法确定原试液中是否含有Fe3+、K+ | |
| B. | 滤液X中大量存在的阳离子有NH4+、Fe3+、H+和Al3+ | |
| C. | 无法确定沉淀B的成分 | |
| D. | 原溶液中一定存在的离子为NH4+、Fe2+、NO3-、SO42- |
| A. | 1molCO2通入750mL 2mol/LKOH溶液中:(K+)=2 c(CO32-)+c(HCO3-)+c(H2CO3) | |
| B. | 加入铝粉有气泡产生的溶液中存在离子:Na+、NH4+、Fe2+、NO3- | |
| C. | 等物质的量Na2CO3、Ca(OH)2、HCl物质混合反应的离子方程式:CO32-+Ca2++H++OH-=CaCO3↓+H2O | |
| D. | Ca与O元素形成化合物中只有离子键 |