题目内容
在t ℃时,将a g NH3完全溶解于水,得V mL饱和溶液,测得该溶液的密度为ρg·cm-3,质量分数为w,其中n(A.溶液中c(OH-)=![]() mol·L-1?
mol·L-1?
B.溶质的物质的量浓度c=![]() mol·L-1?
mol·L-1?
C.溶质的质量分数w=![]() ×100%?
×100%?
D.上述溶液中再加入V mL水后,所得溶液质量分数小于0.5w?
C?
解析:依据电荷守恒n(![]() )+n(H+)=n(OH-)
)+n(H+)=n(OH-)
b+c(H+)×V×10-3=c(OH-)×V×10-3![]() c(OH-)=
c(OH-)=![]() mol·L-1,A正确;
mol·L-1,A正确;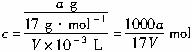 ,
,
B正确;w=![]() ×100%,C错误;等体积混合浓度不同的同种溶液,质量分数偏向于密度大的溶液,水可以看作质量分数为0的氨水,所以D正确。
×100%,C错误;等体积混合浓度不同的同种溶液,质量分数偏向于密度大的溶液,水可以看作质量分数为0的氨水,所以D正确。

练习册系列答案
相关题目
在T ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·cm-3,溶质的质量分数为w,其中含NH4+的物质的量为b mol。下列叙述中正确的是
A.溶质的质量分数为w= ×100% ×100% |
| B.溶质的物质的量浓度c=1000a/17a mol·L-1 |
| C.溶液中c(OH-)=1000b/V mol·L-1 |
| D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w |
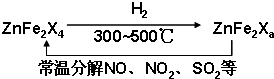
 ×100%
×100%  mol/L
mol/L mol/L
mol/L