题目内容
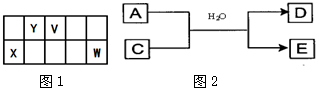
V、W、X、Y、Z是原子序数依次增大的五种短周期元素,V的原子序数与X的原子序数之和等于Y的原子序数,W的原子序数与X的原子序数之和等于Z的原子序数;V和Y位于同一主族,且Y是一种非金属元素.
(1)比较X、Y、Z的原子半径大小
(2)W与Z形成的单质分别为甲、乙,最简单氢化物分别为丙、丁,下列判断正确的是
a.稳定性:甲>乙,沸点:丙>丁 b.活泼性:甲>乙,沸点:丁>丙
c.稳定性:丙<丁,沸点:甲<乙 d.稳定性:丙>丁,沸点:甲>乙
(3)研究表明:VX2在一定条件下可被还原为晶莹透明的晶体M,其结构中原子的排列为正四面体,请写出M及其2种同素异形体的名称
(4)工业上,将Al2O3、V单质、W单质按物质的量之比1:3:1在高温下反应可制得一种无机非金属材料AlW,该反应的化学方程式为
(5)新型纳米材料ZnFe2Xa可由化合物ZnFe2X4经高温还原制得,常温下,它能使工业废气中的酸性氧化物分解除去,转化流程如图所示:
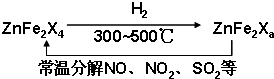
若2mol ZnFe2X a与SO2反应可生成0.75mol S,a=
(6)在t℃时,将a g NH3完全溶于X的常见氢化物,得到V mL溶液,假如该溶液的密度为d g/cm3,质量分数为w,其中含NH4+的物质的量为b mol.下列叙述正确的是
A.溶质的质量分数为w=
B.氨水的物质的量浓度为
mol/L
C.溶液中c(OH-)=
mol?L-+c(H+)
D.上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5w.
(1)比较X、Y、Z的原子半径大小
Si
Si
>P
P
>O
O
(填写元素符号);(2)W与Z形成的单质分别为甲、乙,最简单氢化物分别为丙、丁,下列判断正确的是
a
a
a.稳定性:甲>乙,沸点:丙>丁 b.活泼性:甲>乙,沸点:丁>丙
c.稳定性:丙<丁,沸点:甲<乙 d.稳定性:丙>丁,沸点:甲>乙
(3)研究表明:VX2在一定条件下可被还原为晶莹透明的晶体M,其结构中原子的排列为正四面体,请写出M及其2种同素异形体的名称
金刚石
金刚石
、足球烯
足球烯
、石墨
石墨
;(4)工业上,将Al2O3、V单质、W单质按物质的量之比1:3:1在高温下反应可制得一种无机非金属材料AlW,该反应的化学方程式为
Al2O3+3C+N2=2AlN+3CO
Al2O3+3C+N2=2AlN+3CO
,当0.2mol W单质参加反应,转移电子数目是1.2NA
1.2NA
(5)新型纳米材料ZnFe2Xa可由化合物ZnFe2X4经高温还原制得,常温下,它能使工业废气中的酸性氧化物分解除去,转化流程如图所示:
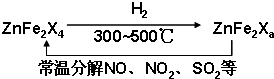
若2mol ZnFe2X a与SO2反应可生成0.75mol S,a=
3.25
3.25
;2molZnFe2Xa可分解物质的量之比为3:2的NO2、NO混合气体(均分解为N2)的体积V=21
21
L(标准状况)(6)在t℃时,将a g NH3完全溶于X的常见氢化物,得到V mL溶液,假如该溶液的密度为d g/cm3,质量分数为w,其中含NH4+的物质的量为b mol.下列叙述正确的是
C
C
A.溶质的质量分数为w=
| a |
| Vd-a |
B.氨水的物质的量浓度为
| 1000a |
| 35V |
C.溶液中c(OH-)=
| 1000b |
| V |
D.上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5w.
分析:V、W、X、Y、Z是原子序数依次增大的五种短周期元素.V的原子序数与X的原子序数之和等于Y的原子序数,V和Y位于同一主族,且Y是一种非金属元素,则Y不可能为氢元素,所以V和Y的原子序数相差8,故X的原子序数为8,则X为氧元素;Y的最外层电子数≥4,即Y的原子序数≥14;W的原子序数与X的原子序数之和等于Z的原子序数,则W,Z的原子序数相差8,W、Z不可能处于同一周期,W的原子序数不可能为1,所以W、Z不可能是氢与氟组合,故W、Z也处于同一族,W的原子序数小于8,则Z的原子序数小于16,由于原子序数Z>Y,故Y为硅元素,Z为磷元素,则V为碳元素,W为氮元素.
解答:解:V、W、X、Y、Z是原子序数依次增大的五种短周期元素.V的原子序数与X的原子序数之和等于Y的原子序数,V和Y位于同一主族,且Y是一种非金属元素,则Y不可能为氢元素,所以V和Y的原子序数相差8,故X的原子序数为8,则X为氧元素;Y的最外层电子数≥4,即Y的原子序数≥14;W的原子序数与X的原子序数之和等于Z的原子序数,则W,Z的原子序数相差8,W、Z不可能处于同一周期,W的原子序数不可能为1,所以W、Z不可能是氢与氟组合,故W、Z也处于同一族,W的原子序数小于8,则Z的原子序数小于16,由于原子序数Z>Y,故Y为硅元素,Z为磷元素,则V为碳元素,W为氮元素.
(1)由上述分析可知,X为氧元素,Y为硅元素,Z为磷元素,同周期随原子序数增大,原子半径减小,所以原子半径Si>P,电子层越多,原子半径越大,所以原子半径P>O,故原子半径Si>P>O,故答案为:Si;P;O;
(2)W为氮元素,Z为磷元素;W与Z形成的单质分别为甲为氮气、乙为磷单质,最简单氢化物分别为丙为NH3、丁为PH3.
a.氮气比磷单质稳定,即稳定性甲>乙;氨气中存在氢键,沸点高,即丙>丁,故a正确;
b.氮气比磷单质稳定,即活泼性甲<乙;氨气中存在氢键,沸点高,即丙>丁,故b正确;
c.元素非金属性N>P,氢化物稳定性丙>丁;通常氮气为气体,磷单质为固体,沸点:甲<乙,故c错误;
d.元素非金属性N>P,氢化物稳定性丙>丁;通常氮气为气体,磷单质为固体,沸点:甲<乙,故d错误;
故选:a;
(3)VX2为CO2一定条件下可被还原为晶莹透明的晶体M,其结构中原子的排列为正四面体,出M及其同素异形体有:金刚石、足球烯、石墨等,
故答案为:金刚石、足球烯、石墨;
(4)工业上,将Al2O3、C单质、N2单质按物质的量之比1:3:1在高温下反应可制得一种无机非金属材料AlN,该反应的化学方程式为 Al2O3+3C+N2=2AlN+3CO;反应中C为还原剂,氮气为氧化剂,碳元素化合价由0价升高为+2价,当0.2molN2参加反应,转移电子数目为0.2mol×3×2×NAmol-1=1.2NA,
故答案为:Al2O3+3C+N2=2AlN+3CO;1.2NA;
(5)X为氧元素,新型纳米材料ZnFe2Oa可由化合物ZnFe2O4经高温还原制得,若2mol ZnFe2O a与SO2反应可生成0.75molS,则ZnFe2O a被还原为ZnFe2O4,令中铁元素的化合价为x,根据电子转移守恒,可知2mol×2×(3-x)=0.75mol×4,解得,x=2.25,利用化合价代数和为,2+2.25×2=2a,解得a=3.25;2molZnFe2Xa可分解物质的量之比为3:2的NO2、NO混合气体(均分解为N2),反应中NO2、NO被还原,ZnFe2Xa被氧化为ZnFe2O4,令NO2、NO的物质的量分别为3ymol、2ymol,根据电子转移守恒有3ymol×4+2ymol×2=2mol×2×(3-2.25),解得y=
,所以NO2、NO混合气体的体积V=
×5mol×22.4L/mol=21L.
故答案为:3.25;21;
(6)X的常见氢化物为H2O,在t℃时,将a g NH3完全溶于水,得到VmL溶液,假如该溶液的密度为d g/cm3,质量分数为w,其中含NH4+的物质的量为b mol.
A.溶质的质量分数为w=
,故A错误;
B.溶质为NH3,氨水的物质的量浓度为c=
mol/L=
mol/L,故B错误;
C.根据电荷守恒可知,溶液中c(OH-)=
mol?L-+c(H+),故C正确;
D.上述溶液中再加入VmL水后,水的密度比氨水大,混合后质量大于原溶液的2倍,氨气质量不变,所得溶液的质量分数小于0.5w,故D错误.
故答案为:C.
(1)由上述分析可知,X为氧元素,Y为硅元素,Z为磷元素,同周期随原子序数增大,原子半径减小,所以原子半径Si>P,电子层越多,原子半径越大,所以原子半径P>O,故原子半径Si>P>O,故答案为:Si;P;O;
(2)W为氮元素,Z为磷元素;W与Z形成的单质分别为甲为氮气、乙为磷单质,最简单氢化物分别为丙为NH3、丁为PH3.
a.氮气比磷单质稳定,即稳定性甲>乙;氨气中存在氢键,沸点高,即丙>丁,故a正确;
b.氮气比磷单质稳定,即活泼性甲<乙;氨气中存在氢键,沸点高,即丙>丁,故b正确;
c.元素非金属性N>P,氢化物稳定性丙>丁;通常氮气为气体,磷单质为固体,沸点:甲<乙,故c错误;
d.元素非金属性N>P,氢化物稳定性丙>丁;通常氮气为气体,磷单质为固体,沸点:甲<乙,故d错误;
故选:a;
(3)VX2为CO2一定条件下可被还原为晶莹透明的晶体M,其结构中原子的排列为正四面体,出M及其同素异形体有:金刚石、足球烯、石墨等,
故答案为:金刚石、足球烯、石墨;
(4)工业上,将Al2O3、C单质、N2单质按物质的量之比1:3:1在高温下反应可制得一种无机非金属材料AlN,该反应的化学方程式为 Al2O3+3C+N2=2AlN+3CO;反应中C为还原剂,氮气为氧化剂,碳元素化合价由0价升高为+2价,当0.2molN2参加反应,转移电子数目为0.2mol×3×2×NAmol-1=1.2NA,
故答案为:Al2O3+3C+N2=2AlN+3CO;1.2NA;
(5)X为氧元素,新型纳米材料ZnFe2Oa可由化合物ZnFe2O4经高温还原制得,若2mol ZnFe2O a与SO2反应可生成0.75molS,则ZnFe2O a被还原为ZnFe2O4,令中铁元素的化合价为x,根据电子转移守恒,可知2mol×2×(3-x)=0.75mol×4,解得,x=2.25,利用化合价代数和为,2+2.25×2=2a,解得a=3.25;2molZnFe2Xa可分解物质的量之比为3:2的NO2、NO混合气体(均分解为N2),反应中NO2、NO被还原,ZnFe2Xa被氧化为ZnFe2O4,令NO2、NO的物质的量分别为3ymol、2ymol,根据电子转移守恒有3ymol×4+2ymol×2=2mol×2×(3-2.25),解得y=
| 3 |
| 16 |
| 3 |
| 16 |
故答案为:3.25;21;
(6)X的常见氢化物为H2O,在t℃时,将a g NH3完全溶于水,得到VmL溶液,假如该溶液的密度为d g/cm3,质量分数为w,其中含NH4+的物质的量为b mol.
A.溶质的质量分数为w=
| a |
| Va |
B.溶质为NH3,氨水的物质的量浓度为c=
| ||
| V×10-3L |
| 1000a |
| 17V |
C.根据电荷守恒可知,溶液中c(OH-)=
| 1000b |
| V |
D.上述溶液中再加入VmL水后,水的密度比氨水大,混合后质量大于原溶液的2倍,氨气质量不变,所得溶液的质量分数小于0.5w,故D错误.
故答案为:C.
点评:本题考查原子结构与位置关系、元素周期律、氧化还原反应、溶液计算等,难度较大,推断元素是关键,充分利用原子序数的关系及元素性质,结合元素周期表结构进行推断.

练习册系列答案
相关题目