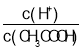��Ŀ����
����Ŀ��Ϊ̽����������Է�Ӧ��mA(g)��nB(g)![]() cZ(g)��H��Ӱ�죬��A��B�����ʵ���֮��Ϊm��n��ʼ��Ӧ��ͨ��ʵ��õ���ͬ�����·�Ӧ�ﵽƽ��ʱZ�����ʵ���������ʵ������ͼ��ʾ�������ж���ȷ���ǣ� ��
cZ(g)��H��Ӱ�죬��A��B�����ʵ���֮��Ϊm��n��ʼ��Ӧ��ͨ��ʵ��õ���ͬ�����·�Ӧ�ﵽƽ��ʱZ�����ʵ���������ʵ������ͼ��ʾ�������ж���ȷ���ǣ� ��
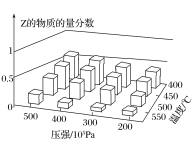
A.��H>0
B.m��n<c
C.�����¶ȣ������淴Ӧ���ʶ�����ƽ�ⳣ����С
D.���º�ѹʱ�����Ѵ�ƽ�����ϵ�м�������Z(g)���ٴδﵽƽ���Z�����ʵ�����������
���𰸡�C
��������
A. ��ͼ���֪���¶����ߣ�Z�����ʵ��������������ͣ�˵������Ӧ�Ƿ��ȵģ�����H��0����A����
B. ����Ӧ�Ƿ��ȵģ�����H��0����Сѹǿ����ѧƽ������������ϵ�������ӵķ�����еģ�������m+n��c����B����
C. �����¶����淴Ӧ���ʶ��ӿ죬��������Ӧ�Ƿ��ȷ�Ӧ������ƽ�ⳣ����С����C��ȷ��
D. �ں��º��������£����Ѵﵽƽ�����ϵ�м�������Z(g)���൱������ѹǿ��ƽ�������ƶ�����Z�ĺ�������D����
��ȷ����C��

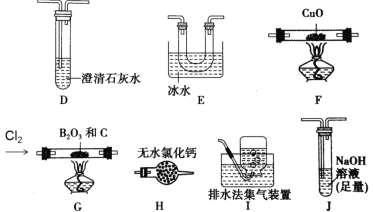
����Ŀ��������ͼ��ʾװ�ý�������ʵ�飬�ܵó���Ӧʵ����۵��ǣ� ��
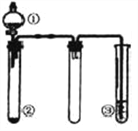
ѡ�� | �� | �� | �� | ʵ����� |
A | ϡ���� | CaCO3 | Na2SiO3��Һ | �ǽ�����:Cl>C>Si |
B | Ũ���� | ���� | Ba(NO3)2��Һ | ��֤SO2������Ա��ο����ɰ�ɫ���� |
C | Ũ��ˮ | ��ʯ�� | ��̪��Һ | ������ˮ��Һ�ʼ��� |
D | Ũ���� | Fe | NaOH��Һ | ����Ũ���ᷴӦ������NO2 |
A. A B. B C. C D. D