题目内容
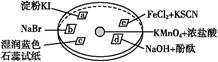
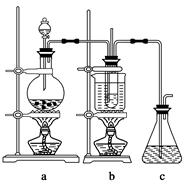
如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是( )
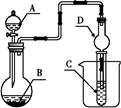

| A.若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色 |
| B.若A为醋酸,B为贝壳,C中盛CaCl2溶液,则C中溶液变浑浊 |
C.若A为浓硝酸,B为铜,C中盛KI 淀粉溶液,则C中溶液变蓝 淀粉溶液,则C中溶液变蓝 |
| D.若A为浓硫酸,B为Na2SO3固体,C中盛石蕊试液,则C中溶液先变红后褪色 |
C
A项不加热,不产生氯气,A项错误;B项将CO2通入CaCl2溶液中,两者不反应,不会产生沉淀,B项错误;Cu与浓HNO3反应放出NO2气体,NO2有氧化性,通入KI淀粉溶液中能生成I2,遇淀粉变蓝色,C项正确;SO2为酸性气体,只能使石蕊变红,不能漂白石蕊,D项错误。

练习册系列答案
相关题目
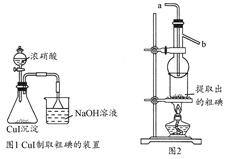
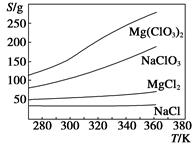
 5NaCl+NaClO3+3H2O,请推测在加热NaClO溶液时发生反应的化学方程式:______________________________。
5NaCl+NaClO3+3H2O,请推测在加热NaClO溶液时发生反应的化学方程式:______________________________。