题目内容
19.在标准状况下,由CO和CO2组成的混合气体的密度为1.607g/L,混合气体的平均相对分子质量是36,此混合物中CO和CO2物质的量之比是1:1.分析 在标准状况下,由CO和CO2组成的混合气体的密度为1.607g/L,所以混合气体的平均相对分子质量是1.607g/L×22.4L/mol=36,设混合物中CO和CO2物质的量分别为xmol,ymol根据相对分子质量求混合物中CO和CO2物质的量之比,由此分析解答.
解答 解:在标准状况下,由CO和CO2组成的混合气体的密度为1.607g/L,所以混合气体的平均相对分子质量是1.607g/L×22.4L/mol=36,设混合物中CO和CO2物质的量分别为xmol,ymol,所以$\frac{28x+44y}{x+y}=36$,所以x;y=1:1,故答案为:36;1:1.
点评 本题考查物质的量有关计算,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
9.下列有关电化学的说法不正确的是( )
| A. | Zn具有还原性和导电性,可用作锌锰干电池的负极材料 | |
| B. | 锂碘电池的总反应为2Li(s)+I2(s)═2LiI(s),则碘电极作该电池的负极 | |
| C. | 铅蓄电池放电时的负极和充电时的阳极均发生氧化反应 | |
| D. | 锌与稀硫酸反应时,要加大反应速率,可滴加少量硫酸铜 |
7.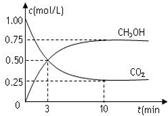 在一恒温恒容密闭容器中充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示.下列说法错误的是( )
在一恒温恒容密闭容器中充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示.下列说法错误的是( )
 在一恒温恒容密闭容器中充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示.下列说法错误的是( )
在一恒温恒容密闭容器中充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示.下列说法错误的是( )| A. | 该密闭容器的体积为1L | |
| B. | 反应达平衡,氢气的转化率为0.75 | |
| C. | 反应达平衡,氢气平均反应速率0.075mol/(L•min) | |
| D. | CO2或H2O物质的量不再改变时反应达平衡 |
14.已知:C(s)+2H2(g)→CH4(g)△H1
C(s)+$\frac{1}{2}$H2(g)→$\frac{1}{2}$C2H2(g)△H2
C(s)+H2(g)→$\frac{1}{2}$C2H4(g)△H3
C2H2(g)+H2(g)→C2H4(g)△H4=-26KJ•mol-1
$\frac{1}{2}$C2H4(g)+H2(g)→CH4(g)△H5=-20KJ•mol-1
下列关系正确的是( )
C(s)+$\frac{1}{2}$H2(g)→$\frac{1}{2}$C2H2(g)△H2
C(s)+H2(g)→$\frac{1}{2}$C2H4(g)△H3
C2H2(g)+H2(g)→C2H4(g)△H4=-26KJ•mol-1
$\frac{1}{2}$C2H4(g)+H2(g)→CH4(g)△H5=-20KJ•mol-1
下列关系正确的是( )
| A. | △H1>△H2 | B. | △H1>△H3 | C. | △H2>△H3 | D. | △H3>△H1>△H2 |
4.下面叙述正确的是( )
| A. | 工业上用过量的碳还原二氧化硅而得到作为半导体材料的硅 | |
| B. | 二氧化硅除可用于制作光学镜片、石英坩埚外,还可用于制造光导纤维 | |
| C. | 水玻璃中加入少量盐酸出现白色沉淀,盐酸过量时,沉淀溶解 | |
| D. | 在Si+2NaOH+H2O═Na2SiO3+2H2↑反应中,NaOH和水均作氧化剂 |
14.下列物质在一定条件下均能产生氧气,其中最适合用于宇航员(宇航员呼吸所需的氧气主要来自太空服中的呼吸面具)出舱时的供氧剂的是( )
| A. | HNO3 | B. | H2O2 | C. | KClO3 | D. | Na2O2 |
