题目内容
已知:相同温度下Ka(HF)﹥Ka(HCN)。现有物质的量浓度和体积均相同的NaF和NaCN两种溶液,已知前者溶液中所含离子数目为n1,后者溶液中所含离子数目为n2,下列关系正确的是( )
| A.溶液pH:NaF﹥NaCN | B.n1 ﹥ n2 | C.n1﹤ n2 | D.c(F-)﹤c(CN-) |
B
NaF溶液中存在Na+ H+ F— OH—,且F— + OH— = Na+ + H+
NaCN溶液中存在Na+ H+ CN— OH— ,且CN— + OH— = Na+ + H+
所以只要比较两者溶液中的c(H+)即可比较n1 、n2大小。
越弱越水解,由水解方程式知道:F— +H2O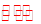 HF + OH— CN— +H2O
HF + OH— CN— +H2O 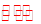 HCN + OH—,即NaCN水解程度大,溶液的碱性强,c(H+)小,故NaCN溶液中离子浓度小。B正确。
HCN + OH—,即NaCN水解程度大,溶液的碱性强,c(H+)小,故NaCN溶液中离子浓度小。B正确。
NaCN溶液中存在Na+ H+ CN— OH— ,且CN— + OH— = Na+ + H+
所以只要比较两者溶液中的c(H+)即可比较n1 、n2大小。
越弱越水解,由水解方程式知道:F— +H2O
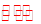 HF + OH— CN— +H2O
HF + OH— CN— +H2O 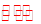 HCN + OH—,即NaCN水解程度大,溶液的碱性强,c(H+)小,故NaCN溶液中离子浓度小。B正确。
HCN + OH—,即NaCN水解程度大,溶液的碱性强,c(H+)小,故NaCN溶液中离子浓度小。B正确。
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

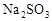


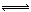 H++A2-,已知常温下浓度为0.1mol/L的H2A溶液中c(H+)=0.11mol/L,则关于0.1mol/L的NaHA溶液的下列叙述中正确的是:( )
H++A2-,已知常温下浓度为0.1mol/L的H2A溶液中c(H+)=0.11mol/L,则关于0.1mol/L的NaHA溶液的下列叙述中正确的是:( )