题目内容
【题目】下列图示与对应的叙述相符的是

A.用硝酸银溶液滴定等浓度的A-、B-、C-的混合溶液(均与Ag+反应生成沉淀),由图1可确定首先沉淀的是C-
B.图2表示反应中某反应物的正、逆反应速率随温度变化的情况, 由图可知该反应的正反应是吸热反应
C.图3表示一定条件下,X(g)![]() Y(g)+Z(s)中物质的量分数随起始投料比变化。m点对应的X转化率为33.3%
Y(g)+Z(s)中物质的量分数随起始投料比变化。m点对应的X转化率为33.3%
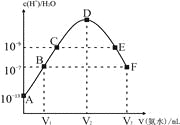
D.图4表示常温下稀释pH相同的HA与盐酸时溶液pH与加入水体积的关系,则HA为弱酸,且a点Kw的数值比b点的大
【答案】C
【解析】
A. 用硝酸银溶液滴定等浓度的A-、B-、C-的混合溶液(均与Ag+反应生成沉淀),由图1可确定A-的浓度最小,则首先沉淀的是A-,A选项错误。
B. 图2表示反应中某反应物的正、逆反应速率随温度变化的情况,由图可知温度升高,最终A的逆反应速率大,说明平衡逆向移动,从而说明该反应的正反应是放热反应,B选项错误。
C. 图3表示一定条件下,X(g)![]() Y(g)+Z(s)中物质的量分数随起始投料比变化。设m点时X的变化量为a,
Y(g)+Z(s)中物质的量分数随起始投料比变化。设m点时X的变化量为a,
X(g)![]() Y(g)+Z(s)
Y(g)+Z(s)
起始量 3 1
变化量 a a
平衡量 3-a 1+a
则有3-a=1+a a=1
对应的X转化率为![]() =33.3%,C正确。
=33.3%,C正确。
D. 图4表示常温下稀释pH相同的HA与盐酸时溶液pH与加入水体积的关系,则HA为弱酸;但a点Kw的数值与b点的相同,因为温度不变,KW不变。D选项错误。
故选C。

练习册系列答案
相关题目