题目内容
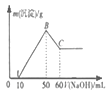
【题目】用碱性氢氧燃料电池为电源进行电解的实验装置示意图如图所示。下列说法中正确的是( )

A.燃料电池工作时负极反应为:H2=2H++2e-
B.若要实现铁上镀铜,则a极是铁,b极是铜
C.若要实现电解精炼粗铜,则a极发生氧化反应,b极上有铜析出
D.a、b两极均是石墨时,在相同条件下,当电池中消耗H222.4L(标准状况)时,a极析出铜64g
【答案】C
【解析】
分析原电池或电解池类试题的实验装置时,解题的切入点是正负极的判断。从图中可以看出,左边电池为燃料电池,右边电池为电解池。通H2的电极为负极,通O2的电极为正极;右边装置中,a电极为阳极,b电极为阴极。
A. 燃料电池工作时负极反应式为:H2-2e-+2OH-=2H2O,错误;
B. 若要实现铁上镀铜,则a极是铜,b极是铁,错误;
C. 若要实现电解精炼粗铜,则a极为阳极,失电子,发生氧化反应,b极为阴极,Cu2+得电子,有铜析出,正确;
D. a、b两极均是石墨时,在相同条件下当电池中消耗H222.4L(标准状况)时,线路中转移电子为2mol,b极为阴极,析出铜64g,a极为阳极,不能析出铜,错误。
故答案为C。

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
【题目】下表是几种弱酸常温下的电离平衡常数:
CH3COOH | H2CO3 | H2S | H3PO4 |
1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
则下列说法中不正确的是( )
A. 碳酸的酸性强于氢硫酸
B. 多元弱酸的酸性主要由第一步电离决定
C. 常温下,加水稀释醋酸,![]() 增大
增大
D. 向弱酸溶液中加少量NaOH溶液,电离常数不变