题目内容
2.某溶液中含有CO32-、Cl-、Na+、NO3-四种离子,若向其中通入足量的HCl气体(溶液体积变化忽略不计).溶液中离子浓度保持不变的是( )| A. | CO32-、NO3- | B. | Na+、Cl- | C. | Na+、NO3- | D. | Cl-、Na+、NO3- |
分析 CO32-、Cl-、Na+、NO3-四种离子中能与盐酸反应的为CO32-,通入HCl,Cl-增大,以此解答该题.
解答 解:CO32-、Cl-、Na+、NO3-四种离子中能与盐酸反应的为CO32-,通入HCl,Cl-增大,Na+、NO3-浓度不变,
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
12.下列说法不正确的是( )
| A. | 碘易升华,应该密封保存 | |
| B. | 液溴应保存在磨口玻璃塞深棕色细口试剂瓶中,并加少量水进行水封 | |
| C. | 酒精与水互溶,所以不能用酒精把碘从碘水中萃取出来 | |
| D. | 用加热的方法可以将NH4Cl与碘的混合物分离 |
13.设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 1mol丙烷分子中,含有的非极性共价键数目为NA | |
| B. | 标准状况下,1.8gH2O分子中所含有的电子数为NA | |
| C. | 25℃时,pH=13的 Ba(OH)2溶液中含有的OH-数目为0.1 NA | |
| D. | 2.24L 氯气与过量的氢氧化钠溶液完全反应转移的电子数为0.1NA |
10.下列关于硫及其化合物的说法中正确的是( )
| A. | SO2和Cl2混合通入水中后可能使品红褪色 | |
| B. | 二氧化硫的排放会导致光化学烟雾和酸雨的产生 | |
| C. | 单质硫在自然界只以化合态存在 | |
| D. | 浓硫酸可用来干燥SO2、CO、Cl2等气体 |
17.下列物质中属于碱性氧化物的是( )
| A. | SO2 | B. | CaO | C. | CO | D. | NaOH |
7.在一定条件下,7g炭粉与14g氧气完全反应生成21g氧化物,则生成物中CO与CO2的物质的量之比是( )
| A. | 1:1 | B. | 2:1 | C. | 2:3 | D. | 3:2 |
4.下列有关物质的性质或应用正确的是( )
| A. | 单质硅用于制造芯片和光导纤维 | |
| B. | 84消毒液的有效成分是NaClO | |
| C. | SO2具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色 | |
| D. | 普通玻璃的组成可用Na2O•CaO•6SiO2表示,是纯净物 |
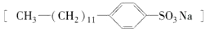 是常用洗涤剂的主要成分.其结构可用图形
是常用洗涤剂的主要成分.其结构可用图形 来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题:
来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题:

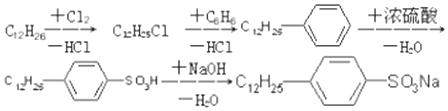
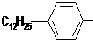 .
. ,反应类型为取代反应.
,反应类型为取代反应.
