题目内容
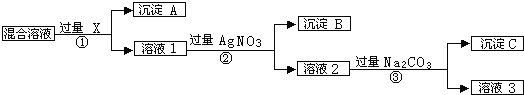
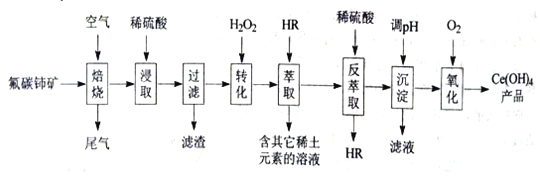
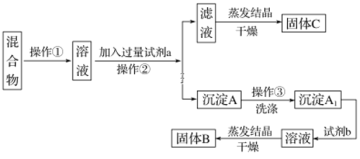
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:
供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(1)操作①的名称是______,操作②的名称是_________。
(2)试剂a是________(填化学式,下同),试剂b是_______,固体B是________。
(3)加入试剂a所发生反应的化学方程式为_______。加入试剂b所发生反应的离子方程式为______。
(4)该方案能否达到实验目的:_____(填“能”或“不能”)。若不能,应如何改进?(若能,此问不用回答)___。
(5)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是____的质量。
【答案】溶解 过滤 K2CO3 HCl BaCl2 K2CO3+BaCl2=BaCO3↓+2KCl BaCO3+2H+=Ba2++CO2↑+H2O 不能 应在操作②的滤液中加入过量盐酸后再蒸发结晶 干燥的沉淀A1或固体B
【解析】
将固体混合物溶解,向溶液中加入碳酸钾,沉淀钡离子,得到碳酸钡沉淀,过滤、洗涤,得到滤液氯化钾,经过蒸发结晶干燥得到KCl固体,沉淀碳酸钡经过洗涤,再加入盐酸溶液得到氯化钡,再蒸发结晶干燥得到BaCl2固体。
(1)混合物变为溶液,因此操作①的名称是溶解,通过图中信息得到沉淀A,说明操作②的名称是过滤;故答案为:溶解;过滤。
(2)氯化钡与碳酸钾反应生成碳酸钡沉淀,因此试剂a是K2CO3,碳酸钡沉淀变为氯化钡,则加入盐酸,因此试剂b是HCl,得到氯化钡溶液后经蒸发结晶干燥得到固体B是BaCl2;故答案为:K2CO3;HCl;BaCl2。
(3)加入试剂a是沉淀钡离子,因此发生反应的化学方程式为K2CO3+BaCl2=BaCO3↓+2KCl。加入试剂b是盐酸和碳酸钡反应生成氯化钡,发生反应的离子方程式为BaCO3+2H+=Ba2++CO2↑+H2O;故答案为;K2CO3+BaCl2=BaCO3↓+2KCl;BaCO3+2H+=Ba2++CO2↑+H2O。
(4)该方案中过滤后滤液中有KCl和K2CO3溶液,因此要先将K2CO3与HCl反应生成氯化钾,再蒸发结晶干燥;故答案为:不能;应在操作②的滤液中加入过量盐酸后再蒸发结晶。
(5)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是含有钡的物质的质量,碳酸钡质量或氯化钡的质量;故答案为:干燥的沉淀A1或固体B。

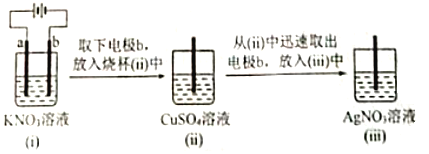
【题目】用多孔石墨电极完成下列实验,下列解释或推断不合理的是( )
实验 |
| ||
现象 | (i)中a、b两极均有气泡产生 | (ii)中b极上析出红色固体 | (iii)中b极上析出灰白色固体 |
A.(i)中,a电极上既发生了化学变化,也发生了物理变化
B.电解一段时间后,(i)中溶液浓度不一定会升高
C.(ii)中发生的反应为H2+Cu2+=2H++Cu↓
D.(iii)中发生的反应只可能是2Ag+Cu=2Ag++Cu2+