题目内容
8.在加入铝粉能放出H2的溶液中,一定能同时大量共存的离子组是( )| A. | K+、Na+、Cl-、SO42- | B. | NH4+、Na+、Cl-、HCO3- | ||
| C. | K+、Na+、NO3-、SO42- | D. | K+、Na+、OH-、SO42- |
分析 加入铝粉能放出H2的溶液,为非氧化性酸或强碱溶液,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答 解:加入铝粉能放出H2的溶液,为非氧化性酸或强碱溶液,
A.酸、碱溶液中该组离子之间均不反应,可大量共存,故A选;
B.碱性溶液中不能大量存在NH4+、HCO3-,酸性溶液中不能大量存在HCO3-,故B不选;
C.酸性溶液中好Al、H+、NO3-发生氧化还原反应不生成氢气,故C不选;
D.酸性溶液中H+、OH-结合生成水,不能大量共存,故C不选;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
19.下表是元素周期表的一部分,针对a~K十一种元素回答下列问题(请用具体化学式回答,否则不给分)
(1)这些元素中非金属性最强的单质是F2,最高价氧化物对应水化物酸性最强的是HClO4,最高价氧化物对应水化物碱性最强的是NaOH.
(2)表中K的氢化物的化学式为HCl,它的还原性比j的氢化物还原性弱(填“强”或“弱”),它水溶液的酸性比j的氢化物水溶液的酸性强(填“强”或“弱”).
(3)e单质为N2,其结构式为N≡N.
(4)用电子式表示h与k构成化合物的形成过程
(5)写出i的氧化物与强碱溶液反应的离子方程式Al2O3+2OH-=2AlO2-+H2O
(6)H2和e的单质化合的反应是可逆反应,且该反应正方向放热.将等物质的量的H2、e的单质充入一恒容密闭容器中,在适当条件下反应.下列说法正确的是ACD(填写选项).
A.升高温度,不论正反应方向还是逆反应方向速率都加快
B.向上述容器中充入适量Ar气可加快反应速率
C.反应过程中,e的单质的体积分数始终为50%
D.反应器内压强不随时间变化而变化,说明反应到达平衡.
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | a | c | d | e | f | g | |
| 3 | b | h | i | j | k |
(2)表中K的氢化物的化学式为HCl,它的还原性比j的氢化物还原性弱(填“强”或“弱”),它水溶液的酸性比j的氢化物水溶液的酸性强(填“强”或“弱”).
(3)e单质为N2,其结构式为N≡N.
(4)用电子式表示h与k构成化合物的形成过程

(5)写出i的氧化物与强碱溶液反应的离子方程式Al2O3+2OH-=2AlO2-+H2O
(6)H2和e的单质化合的反应是可逆反应,且该反应正方向放热.将等物质的量的H2、e的单质充入一恒容密闭容器中,在适当条件下反应.下列说法正确的是ACD(填写选项).
A.升高温度,不论正反应方向还是逆反应方向速率都加快
B.向上述容器中充入适量Ar气可加快反应速率
C.反应过程中,e的单质的体积分数始终为50%
D.反应器内压强不随时间变化而变化,说明反应到达平衡.
3.下列实验过程,无明显现象的是( )
| A. | 二氧化硫通入已酸化的硝酸钡溶液 | |
| B. | 二氧化氮通入氯化亚铁溶液中 | |
| C. | 氢氧化铝沉淀中滴加氨水 | |
| D. | 过量铜片与稀硝酸反应结束的溶液中加入稀硫酸 |
13.下列说法不正确的是( )
| A. | 金刚石、石英和足球烯均为空间网状结构的原子晶体 | |
| B. | 在NaOH、NH4Cl和Na2S04中,都存在离子键和共价键 | |
| C. | 干冰升华的过程只需克服分子间作用力 | |
| D. | H20分解生成H2和O2的过程中既有共价键断裂,又有共价键形成 |
20.下列说法正确的是( )
| A. | 按系统命名法,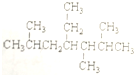 的名称为2,5,6-三甲基-4-乙基庚烷 的名称为2,5,6-三甲基-4-乙基庚烷 | |
| B. | 常压下,正戊烷、异戊烷、新戊烷的沸点依次升高 | |
| C. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| D. | 2-甲基-1,3-丁二烯的键线式为 |
18.下列实验操作正确的是( )
| A. | 将氢氧化钠固体放在滤纸上称量 | |
| B. | 用10 mL量筒量取8.58 mL蒸馏水 | |
| C. | 用强光照射鉴别淀粉胶体与碳酸钠两种无色液体 | |
| D. | 蒸馏时,应将温度计的水银球插入液面以下 |
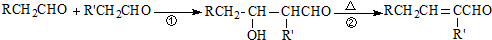
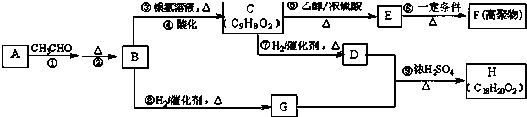
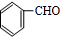 .
.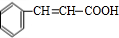 +CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$
+CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$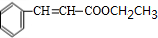 +H2O
+H2O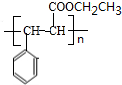
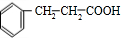 +
+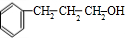 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$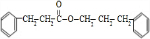 +H2O.
+H2O.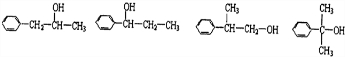 .
.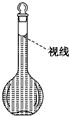 实验室需要配置0.50mol/L NaCl溶液500mL.按下列操作步骤填上适当的文字,以使整个操作完整.
实验室需要配置0.50mol/L NaCl溶液500mL.按下列操作步骤填上适当的文字,以使整个操作完整.