题目内容
某化学反应2A(g) B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
根据上述数据,完成下列填空:
⑴在实验1,反应在20至30分钟时间内用A表示表示该反应的平均速率为________。
⑵在实验2,A的初始浓度c2=____________mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是_______________________________。
⑶设实验3的反应速率为v3,实验1的反应速率为v1,则v3_______v1(填“<”、“=”或“>”),且c3_______1.0 mol/L(填“<”、“=”或“>”)。
⑷比较实验4和实验1,可推测该反应是________反应(选填吸热、放热)。理由是___________________________________________________________。
 B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:| 实验 序号 |   时间 时间浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
⑴在实验1,反应在20至30分钟时间内用A表示表示该反应的平均速率为________。
⑵在实验2,A的初始浓度c2=____________mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是_______________________________。
⑶设实验3的反应速率为v3,实验1的反应速率为v1,则v3_______v1(填“<”、“=”或“>”),且c3_______1.0 mol/L(填“<”、“=”或“>”)。
⑷比较实验4和实验1,可推测该反应是________反应(选填吸热、放热)。理由是___________________________________________________________。
⑴0.O1 mol·L-1·min-1⑵1.0,存在催化剂 ⑶>,>
⑷吸热。达平衡时A的浓度实验4较实验1小,说明升温时平衡逆向正动。
⑷吸热。达平衡时A的浓度实验4较实验1小,说明升温时平衡逆向正动。
试题分析:(1)根据表中数据可知,在实验1,反应在20至30分钟时间内用A表示表示该反应的平均速率为
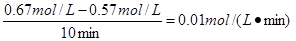 。
。(2)在实验2,温度和平衡时的浓度都与实验1相同,这说明平衡是等效的,所以A的初始浓度c2=1.0mol/L。但反应达到平衡的时间减少,这说明实验2中还隐含的条件是使用了催化剂。
(3)在10min~20min内,实验1和实验3中A 的浓度变化量分别是0.13mol/L和0.17mol/L,所以则v3大于v1。同样c3-0.92>1.0-0.80,所以c3>1.0。
(4)升高温度A的浓度降低,所以升高温度平衡向正反应方向移动,所以正方应是吸热反应。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,有利于培养学生的逻辑推理能力和抽象思维能力,提高学生灵活运用基础知识解决实际问题的能力。

练习册系列答案
相关题目
 3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是 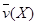 (反应物的消耗速率或产物的生成速率)可表示为
(反应物的消耗速率或产物的生成速率)可表示为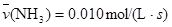
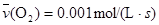
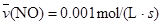
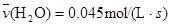
 2AB(g)的△H<0,下列说法正确的是
2AB(g)的△H<0,下列说法正确的是
 (正)_____________
(正)_____________ (g)+5
(g)+5 (g)
(g) 4NO(g)+6
4NO(g)+6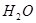 (g)在10L密闭容器中进行,
(g)在10L密闭容器中进行, (NH3)="0.0100" mol·L-1·S-1
(NH3)="0.0100" mol·L-1·S-1