题目内容
【题目】下列说法正确的是( )
A. 某有机物燃烧只生成CO2和H2O,且二者物质的量相等,则此有机物的组成为CnH2n
B. 相同质量的烃完全燃烧,消耗O2越多,烃中含H量越高
C. 一种烃在足量的氧气中燃烧并通过浓H2SO4,减少的总体积就是生成的水蒸气的体积
D. 某气态烃CxHy与足量的氧气恰好完全反应,如果反应前后气体体积不变(温度>100),则y=4;若体积减小,则y>4;否则y<4
【答案】B
【解析】A、由题意可知有机物燃烧后产物只有CO2和H2O,从生成物中含有碳、氢元素,依据质量守恒定律可知该物质中一定含有碳、氢元素,氧元素不能确定,故A错误;B、因为一个碳原子对应消耗一个氧气分子,四个碳原子对应消耗一个氧气分子,而一个碳原子的质量是12个氢原子的质量,12个氢原子消耗三个氧气分子,所以同质量的氢多的肯定消耗氧气多,故B正确;C、烃在氧气中燃烧前后气体的体积可能发生变化,若变化量为x,则一种烃在足量的氧气中燃烧并通过浓H2SO4减少的体积应是生成水蒸气的体积和x之和,故C错误;D、设该烃的化学式为CxHy,根据:CxHy+(x+![]() )O2=xCO2+
)O2=xCO2+![]() H2O,燃烧前后容器内(温度高于100℃)压强保持不变,则气体的物质的量不变,则有体积差为:x+
H2O,燃烧前后容器内(温度高于100℃)压强保持不变,则气体的物质的量不变,则有体积差为:x+![]() -[1+(x+
-[1+(x+![]() )]=
)]= ![]() -1,即可得反应前后体积不变,则y=4;若体积减少则y小于4,反之则大于4,故D错误;故选B。
-1,即可得反应前后体积不变,则y=4;若体积减少则y小于4,反之则大于4,故D错误;故选B。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案【题目】汽车尾气是导致雾霾天气的重要源头之一,其含有的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应。
(一)已知:反应l: N2(g)+O2(g)=2NO(g) △H1 K1
反应2: CO(g)+ 1/2O2(g)=CO2 (g) △H2 K2
反应3: 2NO(g)+2C0(g)=N2(g)+CO2(g) △H3 K3
则反应3的焓变△H3=_______(用△H1和△H2表示) 平衡常数K3=_____(用K1和K2表示)。
(二)向1.0L恒容密闭容器中,充入N2O(g)和C0(g),可发生如下反应:
N2O(g)+C0(g) ![]() N2(g)+CO2(g),所得实验数据如下表:
N2(g)+CO2(g),所得实验数据如下表:
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(N2O) | n(CO) | n(CO2) | ||
① | 400 | 0.20 | 0.30 | 0.14 |
② | 500 | 0.10 | 0.40 | 0.080 |
③ | 500 | 0.30 | 0.20 | A |
④ | 600 | 0.60 | 0.40 | B |
上述实验编号①中,若10min时测得n(N2)=0.12mol,则0至10min内,用CO2表示的平均反应速率以v(CO2)=________;
(2)500℃时,欲使N2O的平衡转化率a(N2O)≥80%,则起始时n(N2O):n(CO)≤______。
(3)上述实验编号④达平衡时,b____0.24(填“>”、“<”或“=”),原因是_______。
(4) N2O(g)+C0(g)![]() N2(g)+CO2(g)的反应体系达到平衡后,各物质的浓度在不同条件下的变化情况如下图所示:
N2(g)+CO2(g)的反应体系达到平衡后,各物质的浓度在不同条件下的变化情况如下图所示:
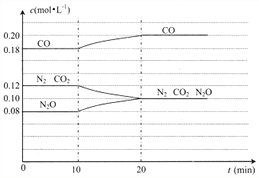
①若在第10min仅改变了一个条件,第20min时是在条件下达到新的平衡状态,则第10min 时改变的条件可能是_______;
②比较CO在第5min和第25min时速率的大小v(5)____v(25)(填”>”、“<”或“= ”),你判断的理由是______________。
【题目】“海绵镍铝催化剂” 是一种多孔的镍铝合金,常用作有机催化剂。现以某粗镍(含Ni、Fe、Cu及难与酸、碱溶液反应的不溶性杂质)为原料制取该催化剂,主要流程如下:
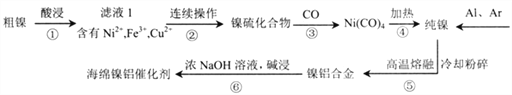
己知:25℃时,以0.1mol/L金属离子测定得到如下数据:
物质 | CuS | Cu(OH)2 | Ni(OH)2 | NiS | Fe(OH)3 | |
Ksp | 6×10-36 | 3×10-19 | ||||
pH | 开始沉淀 | 4.7 | 7.2 | 1.9 | ||
沉淀完全 | 6.7 | 9.2 | 3.2 | |||
根据信息回答:
(1)步骤①常用热浓硫酸进行酸浸,写出酸浸时金属镍发生反应的化学方程式__________。
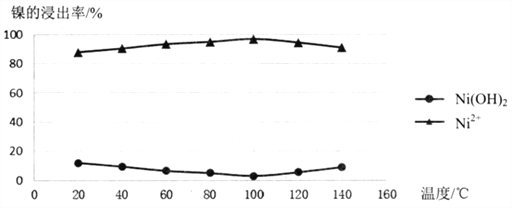
(2)酸浸过程应控制酸的浓度、温度等条件,如图是镍的浸出率与温度的关系,温度高于100℃时,Ni2+浸出率降低的原因可能是______________。
(3)滤液l中含有0.8mol/LNi2+、0.1mol/LFe3+、0.1mol/LCu2+,步骤②的连续操作过程需要先分离出铁元素、铜元素,再制得镍硫化合物。为达到此目的,应先加NaOH将溶液调节至_______(填pH的取值范围);再加_______(选填最佳试剂的序号)。当溶液中Ni2+开始形成NiS时,c(Cu2+)_______。(忽略溶液体积变化)
A.硝酸 B.氨水 C. A12S3 D.H2S
(4)步骤③生成的Ni(CO)4中碳的化合价与KCN中碳的化合价相同,则Ni(CO)4中Ni的化合价为______;工业上也常用NaClO氧化NiSO4,将制得的NiOOH热分解后进行还原得到Ni。ClO-在碱性条件下氧化Ni2+生成NiOOH的离子方程式为_____________。
(5)步骤⑥的目的是降低铝含量、获得多孔状的“海绵镍铝催化剂”,从而增强对氢气的吸附性,步骤⑥的离子方程式为___________________。